Objetivo é aperfeiçoar medidas sanitárias para a operação e o embarque e desembarque de equipes em plataformas e em embarcações de carga.
A Anvisa decidiu realizar diligências, por um período de 10 dias, para o levantamento de informações necessárias à avaliação sobre alterações nas medidas sanitárias para a operação e o embarque e desembarque de equipes em plataformas e em embarcações de carga situadas em águas marítimas (jurisdicionais) brasileiras. A proposta foi apresentada durante a 3ª Reunião Extraordinária Pública da Dicol de 2022, realizada nesta sexta-feira (28/1), e teve apoio unânime dos diretores da Agência.
A recomendação de realização de diligências partiu do diretor Alex Machado Campos, que ressaltou a importância desse debate diante do avanço da variante Ômicron e seu impacto na pandemia de Covid-19 e no aumento de casos em plataformas de exploração de petróleo e gás natural, além de embarcações.
O objetivo das diligências é fazer uma discussão aprofundada e adequada em torno da norma atual, publicada por meio da Resolução da Diretoria Colegiada (RDC) 584/2021, visando o aperfeiçoamento da regulação sanitária. Para isso, a Agência realizará reuniões com o Ministério da Saúde, Ministério da Economia, Ministério da Integração, Ministério do Trabalho, Ministério Público do Trabalho, Petrobrás e outras empresas do setor regulado, além da representação de trabalhadores e de sociedades médicas, entre outras, buscando subsídios para a tomada de decisão sobre o tema.
A conversão de apresentação e votação de pauta da Dicol em diligência é prevista no artigo 28 da Resolução da Diretoria Colegiada (RDC) 585/2021, que dispõe sobre o Regimento Interno da Anvisa.
Anvisa participa de evento sobre Novas Substâncias Psicoativas
Evento virtual na próxima segunda-feira (31/1), às 11h, irá abordar as Novas Substâncias Psicoativas (NSP). Participe!
Na próxima segunda-feira (31/1), às 11h, a Anvisa participará da inauguração virtual do Subsistema de Alerta Rápido (SAR) do Sistema Nacional de Políticas Públicas sobre Drogas (Sisnad). Na ocasião, será lançado o 1º Informe do SAR. A publicação irá tratar sobre as Novas Substâncias Psicoativas (NSP).
Coordenado pela Secretaria Nacional de Políticas sobre Drogas e Gestão de Ativos (Senad) do Ministério da Justiça e Segurança Pública, o subsistema possibilita a rápida identificação das NSP.
Nesse sentido, é importante esclarecer que esse documento será essencial tanto para as autoridades policiais quanto para as sanitárias, por abordar informações relacionadas às novas drogas em território nacional. Clique aqui e saiba mais sobre as NSP.
Para participar do evento, basta clicar no link abaixo, no dia e horário agendados. Não é preciso fazer cadastro prévio.
Dia 31/1, às 11h – Primeiro Informe do Subsistema de Alerta Rápido Sobre Drogas (SAR)
Anvisa regulamenta a utilização de autotestes para Covid-19
Resolução aprovada estabelece requisitos para registro, distribuição, comercialização e utilização de autotestes.
A Diretoria Colegiada da Anvisa aprovou, nesta sexta-feira (28/1), durante sua 3ª Reunião Extraordinária Pública de 2022, a resolução que estabelece os requisitos e os procedimentos para a solicitação de registro, distribuição, comercialização e utilização de autotestes para detecção do antígeno de Sars-CoV-2.
Acesse aqui o Perguntas Frequentes sobre o tema.
Com a aprovação, será permitida a venda de autotestes diretamente ao consumidor por farmácias e estabelecimentos de saúde licenciados para comercializar dispositivos médicos. Importante deixar claro que é proibida a oferta de autotestes na internet em sítios eletrônicos que não pertençam a farmácias ou estabelecimentos de saúde autorizados e licenciados pelos órgãos de vigilância sanitária competentes.
Atenção! Nenhum autoteste poderá ser comercializado imediatamente no país. As empresas habilitadas legalmente que desejarem colocar esses dispositivos à venda terão que registrar o produto na Anvisa. A Resolução de Diretoria Colegiada (RDC) aprovada hoje estabelece os critérios para o peticionamento do registro, bem como, em seu artigo 22, define que as petições relacionadas ao tema serão analisadas com prioridade pela Agência, enquanto for mantida a declaração de emergência de saúde pública.
Condições
Entre os requisitos, a Anvisa determina que as instruções de uso, armazenagem e descarte do produto sejam claras e que utilizem ilustrações para facilitar o manuseio e a interpretação do resultado por parte do público leigo, ou seja, por indivíduos sem treinamento técnico ou científico formal para uso do produto.
O solicitante do registro do autoteste deve dispor de um canal de atendimento ao usuário, com acesso direto a pessoal capacitado para atender, orientar e encaminhar as demandas sobre o uso do produto e como proceder após a obtenção do resultado. Além de disponibilizar o contato desse serviço de atendimento, a empresa deve indicar o Serviço Disque Saúde do Ministério da Saúde, em conformidade com o Plano Nacional de Expansão da Testagem para Covid-19, o PNE-Teste.
Com relação à embalagem, o rótulo externo do produto deve conter todos os componentes do kit, que são necessários para a realização do teste, e também a validade do dispositivo, de modo a evitar seu uso fora do prazo de validade.
Monitoramento
Os autotestes estão sujeitos ao monitoramento pós-comercialização por meio do Sistema de Notificação e Investigação em Vigilância Sanitária, o Vigipós. O detentor do registro deve se responsabilizar por todas as ações de vigilância pós-comercialização do produto, em todo seu ciclo de vida. Isso inclui o estabelecimento de mecanismos para monitorar e notificar queixas técnicas e eventos adversos, recolhimento do produto quando determinado pela Anvisa ou sempre que houver indícios suficientes de que o dispositivo não atende aos requisitos de qualidade, segurança e desempenho e também notificação de ações de campo decorrentes de eventos adversos associados ao produto.
O setor varejista, por sua vez, deve notificar os eventos adversos e queixas técnicas no Sistema de Notificações em Vigilância Sanitária, o Notivisa. No caso de o usuário notificar problemas relacionados ao uso do produto diretamente à Anvisa, o responsável pelo registro deverá avaliar e responder a demanda no sistema informatizado disponibilizado pela Agência.
Histórico
Em reunião realizada em 19 de janeiro de 2022, a Diretoria Colegiada da Anvisa, ao avaliar a proposta de regulamentação de autotestes, manifestou a necessidade de diligências para esclarecimentos sobre as condicionantes da política pública para utilização desses dispositivos por pessoas leigas.
Segundo entendimento da Procuradoria Federal junto à Anvisa, a nota técnica anteriormente enviada pelo Ministério da Saúde à Agência não cumpria os itens considerados necessários a uma política pública. Por essa razão, foi solicitado pedido de esclarecimento com informações adicionais ao respectivo Ministério.
CONFIRA O RESUMO
- Os autotestes só poderão ser comercializados no país após registro do produto junto à Anvisa.
- A Anvisa analisará os pedidos de registro de autotestes com prioridade.
- É proibida a venda de autotestes em sites que não pertençam a farmácias ou estabelecimentos de saúde autorizados e licenciados pelos órgãos de vigilância sanitária.
- O autoteste não define um diagnóstico, o qual deve ser realizado por profissional de saúde. Seu caráter é orientativo. Ou seja, não se trata de um atestado médico.
- O resultado do autoteste não é válido para viagens e entradas em eventos.
Acesse o Perguntas Frequentes sobre o tema.
Voto da diretora relatora Cristiane Rose Jourdan
Voto do diretor Rômison Rodrigues Mota
Anvisa alerta para diferenças entre as vacinas para crianças
O objetivo é favorecer a vacinação segura das crianças contra Covid-19
A Anvisa publicou um alerta aos profissionais de saúde sobre as diferenças das vacinas contra a Covid-19 para o público infantil.
O documento traz as recomendações de armazenamento, como preparar cada vacina, faixa etária indicada, qual dose deve ser administrada e o tempo de intervalo entre as doses, por exemplo. Isso porque as duas vacinas aprovadas pela Anvisa para crianças (Pfizer e Coronavac) possuem características diferentes em muitos desses aspectos.
O objetivo do alerta é favorecer a vacinação segura das crianças, assim como o alerta anteriormente publicado sobre as vacinas para adultos. A recomendação é que os postos de vacinação imprimam o quadro disponível no alerta e disponibilizem para as equipes. Assim, observando as diferenças entre as vacinas, pode-se reduzir riscos de erros no processo de vacinação.
Clique aqui para imprimir uma versão do cartaz abaixo para impressão.
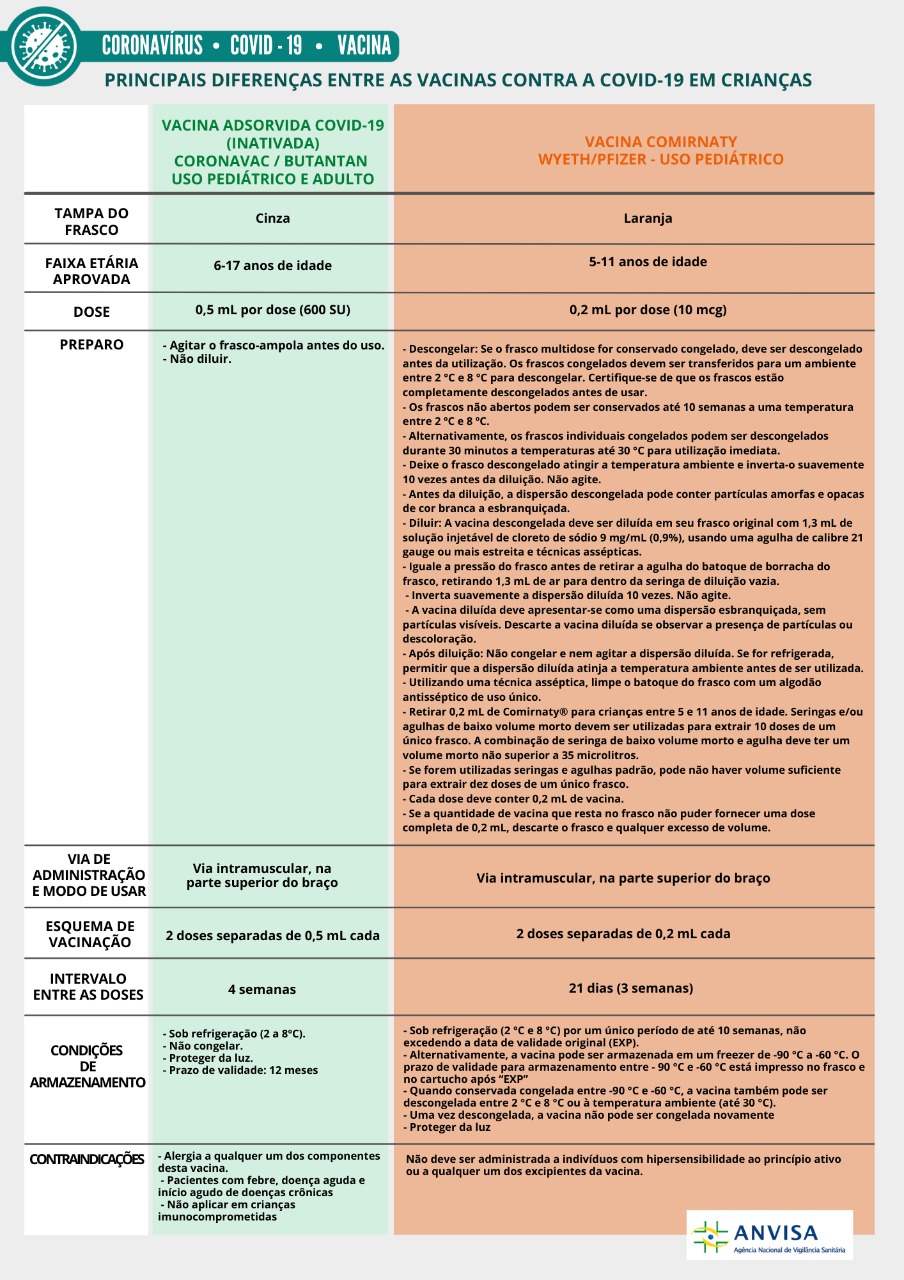
Fonte: Anvisa, em 28.01.2022.
