O encontro é uma continuação da agenda que a Agência ver realizando sobre o tema com todos laboratórios
quem têm vacinas contra Covid-19 em uso no Brasil.
A Anvisa realizou nesta sexta-feira (27/8) reunião com o laboratório Pfizer para tratar da discussão em torno da necessidade ou não de dose de reforço de sua vacina. O encontro é uma continuação da agenda que a Agência ver realizando sobre o tema com todos laboratórios quem têm vacinas contra Covid-19 em uso no Brasil.
Durante a reunião, foram apresentados copilados de dados já públicos. O objetivo da Anvisa é acompanhar todos os dados, tanto aqueles que fazem parte das pesquisas diretas conduzidas pela Pfizer como de outras publicações que possam contribuir para a avaliação sobre a necessidade de uma dose de reforço da vacina. Até o momento, não há dados conclusivos.
Vacina Comirnaty Pfizer: Anvisa certifica mais uma planta fabril
A emissão do CBPF é pré-requisito para que essa fábrica seja incluída no registro da Vacina Comirnaty.
Aequipe técnica da Anvisa concluiu a análise das informações enviadas pela Pfizer para a verificação do cumprimento das Boas Práticas de Fabricação (BPF) para uma nova empresa, visando à inclusão desta empresa na cadeia fabril aprovada no registro da vacina Comirnaty contra a Covid-19.
A empresa EXELEAD, INC. localizada em Indianapolis (IN), nos Estados Unidos da América, será mais uma opção para realizar a etapa de formulação da vacina, aumentando o leque de plantas fabris e ampliando a capacidade produtiva da Comirnaty.
A Certificação de Boas Práticas de Fabricação é feita de forma individual para cada fábrica envolvida no processo fabril e todas as demais empresas requisitadas no registro pela Pfizer já estão devidamente certificadas quanto ao cumprimento das BPF.
A emissão do CBPF é pré-requisito para que essa planta seja incluída no registro da vacina Comirnaty.
Havendo aprovação pelo registro a cadeia fabril passará a ser:
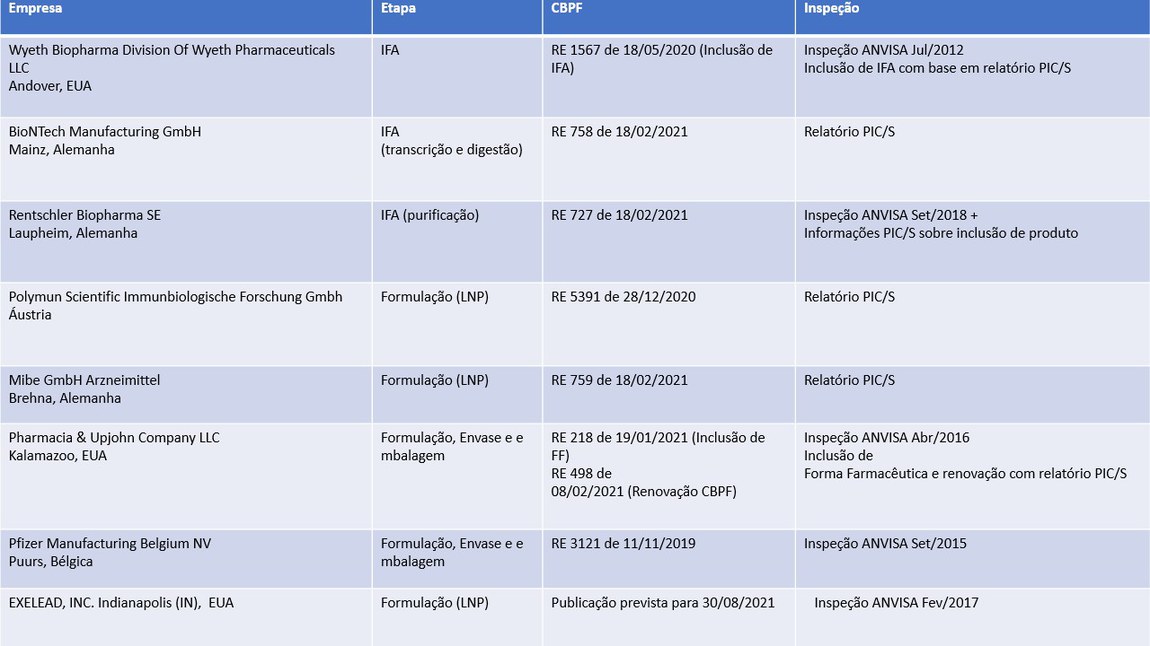
Formas de emitir a certificação
A verificação do cumprimento das boas práticas de fabricação de medicamentos durante a pandemia pode ser realizada por meio de dois diferentes mecanismos, conforme estabelecido pela Resolução RDC 346/2020, com objetivo de aumentar a agilidade, bem como garantir a qualidade dos medicamentos. A primeira é a inspeção realizada pela Anvisa, quando servidores da Agência fazem a inspeção diretamente. A segunda é por meio de relatórios de inspeção elaborados por autoridades reguladoras com equivalência regulatória à agência brasileira. Essas autoridades, junto com a Anvisa, compõem o Esquema de Cooperação de Inspeção Farmacêutica (PIC/S, em sua sigla em inglês).
No caso da planta da Exelead, a Anvisa já tinha conduzido inspeção na empresa para outro produto/demandante, e concluiu o presente pedido avaliando os dados referentes a introdução do novo produto na linha fabril.
PIC/S
Em 1º de janeiro de 2021, a Anvisa se tornou o 54º membro do PIC/S, passando a contar com o reconhecimento internacional da excelência das inspeções em Boas Práticas de Fabricação (BPF) de medicamentos e insumos farmacêuticos de uso humano. Esta iniciativa internacional em inspeção farmacêutica está voltada para duas principais atividades:
Harmonização internacional, por meio do estabelecimento de guias de referência na área de Boas Práticas de Fabricação e de Distribuição de produtos farmacêuticos.
Realização de treinamentos a fim de tornar equivalentes os sistemas de inspeção de boas práticas de fabricação de todo o mundo.
Anvisa faz reunião com a Janssen para discutir dose de reforço
Até o momento, não há dados conclusivos sobre necessidade de dose de reforço da vacina da Janssen,
nem sobre o seu uso como dose de reforço para pessoas que tomaram outras vacinas.
A Anvisa realizou, nesta sexta-feira (27/8), uma reunião com o laboratório Janssen-Cilag para discutir informações sobre o desenvolvimento e o andamento dos estudos sobre doses de reforço de sua vacina.
A Anvisa solicitou que a empresa apresente os dados em processo de submissão contínua, na medida em que forem sendo concluídos. O objetivo é acompanhar todos os dados, tanto aqueles que fazem parte das pesquisas diretas conduzidas pela Janssen, como dados de outras publicações que possam contribuir para a avaliação sobre a necessidade de uma dose de reforço da vacina.
Para a Anvisa, a principal questão neste momento é entender se e quando essas doses serão necessárias, o que pode ter impacto no esquema de imunização em uso no país.
Até o momento, não há dados conclusivos sobre necessidade de dose de reforço da vacina da Janssen, nem sobre o seu uso como dose de reforço para pessoas que tomaram outras vacinas. O imunizante da Janssen é administrado em dose única.
No encontro, ficou acordado que a Anvisa e a Janssen terão uma agenda permanente para acompanhar os dados que estão sendo levantados sobre uma possível dose de reforço.
Uso combinado de medicamentos e informações de bula: entenda
O uso combinado de medicamentos, mesmo que não conste na bula de um deles, não se trata de uso off label.
A Anvisa explica: o uso combinado de medicamentos, apesar de não constar na bula de um deles em alguns casos, não deve ser considerado como uso off label. E por que razão? Pois a eficácia e a segurança dos medicamentos são avaliadas e aprovadas pela Agência, a partir do requerimento de um dos detentores do registro e investigador do uso combinado com outros medicamentos.
Quando os medicamentos combinados são do mesmo detentor do registro, os dados e as informações de indicação, posologia e modo de uso costumam estar presentes nas bulas de todos os medicamentos utilizados em combinação. Vale ressaltar, porém, que o detentor do registro é quem deve solicitar as atualizações dos textos de bula à Anvisa.
Porém, quando o investigador do uso combinado não é o detentor do registro de todos os medicamentos utilizados, não há previsão legal para atualização das bulas dos medicamentos envolvidos, uma vez que os estudos clínicos foram gerados por um terceiro. Nesses casos, apenas a bula do medicamento, cujo detentor do registro foi o responsável pela condução dos estudos clínicos, terá informações sobre o uso combinado incluídas no texto.
Ou seja, a bula de um ou mais medicamentos utilizados em combinação pode não mencionar a indicação ou o uso combinado. Mas certamente a Anvisa analisou os dados, comprovou a eficácia e a segurança da combinação de medicamentos para a respectiva autorização.
Saiba mais
As bulas reúnem uma série de informações a fim de orientar pacientes e profissionais da saúde sobre, por exemplo, dosagem e indicações, modo de uso, composição, contraindicações, reações adversas, interações com outros medicamentos e alimentos, precauções e armazenamento. As informações contidas nas bulas refletem os dados apresentados no dossiê de registro e de alterações pós-registro dos medicamentos, como a inclusão de nova indicação.
Importante observar que as bulas seguem as disposições da Resolução da Diretoria Colegiada (RDC) 47/2009, que estabeleceu as regras para elaboração, harmonização, atualização, publicação e disponibilização de bulas de medicamentos. A norma tem como objetivo aprimorar a forma e o conteúdo das bulas de todos os medicamentos registrados e notificados, comercializados no Brasil, de modo a garantir o acesso à informação segura e adequada em prol do uso racional de medicamentos.
Anvisa atualiza a lista de Denominações Comuns Brasileiras
Ao todo, foram incluídas 57 novas denominações e uma foi alterada.
A Anvisa publicou, no dia 23/8, a Resolução da Diretoria Colegiada (RDC) 535/2021, que atualizou a lista de Denominações Comuns Brasileiras (DCB). Ao todo, foram incluídas 57 novas denominações e uma foi alterada. Confira a lista consolidada das DCB no portal da Agência.
O que são as Denominações Comuns Brasileiras (DCB)?
São as denominações de fármacos ou de princípios farmacologicamente ativos aprovadas pelo órgão federal responsável pela vigilância sanitária (Lei 9.787/1999).
Com a introdução do registro eletrônico, a lista adquiriu uma concepção mais ampla e inclui também a denominação de insumos inativos, soros hiperimunes, vacinas, radiofármacos, plantas medicinais, substâncias homeopáticas e produtos biológicos.
Tais denominações são empregadas nos processos de registro, rotulagem, elaboração de bulas, licitação, importação, exportação, comercialização, propaganda, publicidade, informação, prescrição, dispensação e em materiais de divulgação didáticos, técnicos e científicos em todo o país.
Confira a íntegra da RDC 535/2021 e a lista atualizada.
Fonte: Anvisa, em 27.08.2021.
