Encontro virtual será no dia 27/11, às 15h. Participe!
A Anvisa irá realizar uma videoconferência (webinar) para apresentar os principais pontos do Guia 66/2023. O documento traz orientações às empresas sobre como a Anvisa avalia o potencial mutagênico (de causar alterações genéticas em células) dos agrotóxicos. O encontro será na próxima segunda-feira (27/11), às 15h.
O Guia está aberto a contribuições até o dia 15/4/2024.
Para participar do encontro virtual, basta clicar no link abaixo, no dia e horário agendados. Não é preciso fazer cadastro prévio.
Dia 27/11, às 15h – Webinar sobre o Guia de Avaliação do Potencial Mutagênico de Agrotóxicos - Guia 66/2023
Acompanhe a 18ª Reunião da Dicol nesta quarta-feira (22/11)
Encontro começa às 9h30 e será transmitido ao vivo.
A Anvisa realiza, a partir das 9h30 desta quarta-feira (22/11), a 18ª Reunião Ordinária Pública da Diretoria Colegiada (Dicol) de 2023. O encontro dos diretores será transmitido ao vivo pelo canal da Agência no YouTube.
As minutas das propostas em fase de deliberação podem ser consultadas nesta página. Entre os itens da pauta, está uma proposta para advertências sanitárias e mensagens a serem utilizadas nas embalagens de produtos fumígenos derivados do tabaco, assim como nos expositores e mostruários de venda desses produtos.
Veja aqui a pauta completa e abaixo um resumo de outros temas previstos para a reunião:
- Norma sobre classificação de risco, regimes de notificação e de registro, e requisitos de rotulagem e instruções de uso de dispositivos médicos para diagnóstico in vitro.
- Regras para elaboração, harmonização, atualização, publicação e disponibilização de bulas de medicamentos para pacientes e para profissionais de saúde.
- Boas Práticas de Fabricação Complementares aos Produtos de Terapias Avançadas e proposta de Instrução Normativa para dispor sobre as Boas Práticas em Células Humanas para uso terapêutico e pesquisa clínica.
- Relatório de Análise de Impacto Regulatório sobre análise e deliberação dos recursos administrativos submetidos à Gerência-Geral de Recursos da Anvisa.
- Atualização da Lista de Medicamentos de Baixo Risco sujeitos à notificação.
- Proposta para estabelecer as condições para procedimento otimizado de análise das petições de avaliação na área de alimentos
- Propostas de Relatório de Análise de Impacto Regulatório sobre o marco regulatório das Denominações Comuns Brasileiras (DCBs) e de Consulta Pública de Resolução da Diretoria Colegiada para dispor sobre as regras para estabelecimento de nomenclaturas e atualização da lista das DCBs.
- Avaliação do Parecer do Comitê Gestor que aprova os Planos de Trabalho de 2023 dos Comitês Técnicos Temáticos da Farmacopeia Brasileira e o relatório de atividades dos colegiados da Farmacopeia Brasileira.
- Norma sobre princípios gerais, funções tecnológicas e condições de uso de aditivos alimentares e coadjuvantes de tecnologia em alimentos.
- Propostas para alteração de monografias de ingredientes de agrotóxicos.
- Proposta de Relatório de Análise de Impacto Regulatório sobre o controle sanitário de viajantes em portos, aeroportos e passagens de fronteira.
- Boas Práticas de Cosmetovigilância para empresas titulares da regularização de produtos cosméticos de uso em humanos junto à Anvisa.
- Proposta de norma para alterar os requisitos sanitários para óleos e gorduras vegetais.
- Proposta de alteração da norma sobre a definição, a classificação, os requisitos técnicos para rotulagem e embalagem, os parâmetros para controle microbiológico, bem como os requisitos técnicos e procedimentos para a regularização de produtos de higiene pessoal, cosméticos e perfumes.
- Atualização do Anexo I (Listas de Substâncias Entorpecentes, Psicotrópicas, Precursoras e Outras sob Controle Especial) da Portaria SVS/MS 344, de 12 de maio de 1998.
Acompanhe pelo YouTube da Anvisa.
Anvisa atualiza formulário de solicitação de importação por remessa expressa
Mudanças no sistema Solicita entram em vigor no dia 5/12. Saiba mais.
A partir do próximo dia 5 de dezembro, os formulários dos assuntos de remessa expressa no sistema Solicita serão atualizados.
Com essa atualização, todos os pedidos de importação por meio dessa modalidade passarão a exigir o preenchimento da quantidade de unidades da remessa solicitada.

A alteração permitirá validar a quantidade informada frente ao assunto solicitado, impedindo que o usuário encaminhe solicitações com quantidades divergentes do assunto requerido. Ao identificar uma inconsistência no campo “Quantidade importada”, o sistema apresentará uma mensagem orientando o ajuste do pedido, como demonstrado abaixo.
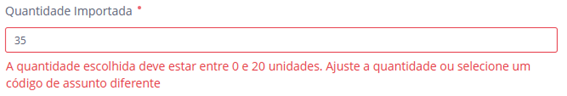
Tal evolução reduzirá o tempo necessário para o atendimento da solicitação. Com a validação, não ocorrerão situações em que será necessário realizar o fluxo de solicitação para complementação de taxa.
Além disso, o campo “Posto de Destino” foi excluído para refletir a centralização dos processos de trabalho.
Remessa expressa de produtos derivados de Cannabis
Para as solicitações de importação de produto derivado de Cannabis, passarão a ser exigidas mais informações, de forma a permitir robustez ao monitoramento dessas importações.
A partir dessa evolução, o solicitante deverá informar:
- Número de conhecimento.
- Quantidade importada.
- Número da Autorização de Importação (campo com 17 caracteres para inserção do número de autorização de importação concedido por meio do serviço “Solicitar autorização para importar produtos derivados de Cannabis”).
- CPF do paciente.
- Endereço do destinatário.
- Nome comercial do produto importado.
- Nome do exportador.
- País do exportador.
O Manual do Sistema Solicita apresenta mais detalhes sobre o preenchimento do formulário.
Operacionalização da mudança
Os ajustes necessários ocorrerão entre as 17h do dia 4/12 e as 12h do dia 5/12, motivo pelo qual os assuntos referentes à remessa expressa ficarão indisponíveis para peticionamento durante esse período.
Fonte: Anvisa, em 21.11.2023.
