Programação contempla dois dias de encontros e visa tratar de atividades de cooperação entre as duas agências.
Nesta terça-feira (17/5), a Anvisa recebe em sua sede, em Brasília (DF), representantes da Agência de Medicamentos da Dinamarca (Danish Medicines Agency – DKMA) e da Embaixada da Dinamarca no Brasil para tratar da retomada de atividades de cooperação. Um segundo encontro está previsto para esta quarta-feira (18/5).
A cooperação técnica entre a Anvisa e a DKMA foi iniciada por meio do primeiro plano de trabalho entre as duas agências, assinado no ano de 2016 e intitulado "Cooperação Setorial Estratégica entre Brasil e Dinamarca para Apoiar a Gestão Eficiente da Saúde no Brasil".
Em 2020, as autoridades assinaram o segundo plano de trabalho, com previsão de realizar atividades em diversas áreas reguladas pelas duas agências. No final do mesmo ano, porém, as atividades foram suspensas em razão da pandemia provocada pelo novo coronavírus.
Por fim, ressalta-se que esses dois dias de evento têm como objetivo reavaliar as atividades programadas, incluir experiências adquiridas na pandemia e adotar um plano de trabalho revisado.
Clique aqui e saiba mais sobre as iniciativas de cooperação e convergência regulatória da Anvisa.


VigiMed passará por nova atualização. Confira as melhorias!
Sistema para gestão de notificações de eventos adversos a medicamentos e vacinas será atualizado nesta terça-feira (17/5).
A Anvisa informa que o VigiMed (VigiFlow®), sistema adotado pela Agência desde 2018 para gestão das notificações de suspeitas de eventos adversos relacionados a medicamentos e vacinas no país, passará por mais uma atualização nesta terça-feira (17/5). As melhorias são promovidas pelo Centro Colaborador da Organização Mundial da Saúde (OMS) para o monitoramento de medicamentos (Uppsala Monitoring Centre – UMC), a partir de análises e debates entre os países colaboradores, incluindo o Brasil.
Uma das principais mudanças foi motivada por demanda da Gerência de Farmacovigilância da Anvisa, a fim de possibilitar que as Vigilâncias Sanitárias (Visas) estaduais participem mais ativamente do processo de farmacovigilância.
É importante observar que, devido às atualizações, o sistema poderá apresentar instabilidades neste 17 de maio.
Saiba mais
Entre as principais melhorias realizadas no VigiMed, estão o compartilhamento automático das notificações de empresas com as Vigilâncias Sanitárias, a incorporação de termos padrão da Direção Europeia da Qualidade dos Medicamentos e Cuidados de Saúde(European Directorate for the Quality of Medicines and Healthcare – EDQM) relacionados à forma farmacêutica e via de administração, além de orientações mais detalhadas às empresas farmacêuticas.
Até então, a configuração das interfaces eReporting vinculavam os casos apenas à Anvisa. A partir de agora, as notificações provenientes das empresas farmacêuticas poderão ser distribuídas automaticamente, por meio do sistema, às Vigilâncias Sanitárias estaduais, permitindo, portanto, o monitoramento conjunto entre a Agência e as Visas. Vale lembrar que esse processo será aprimorado durante a formalização do Sistema Nacional de Farmacovigilância, pauta da Agenda Regulatória 2022-2023.
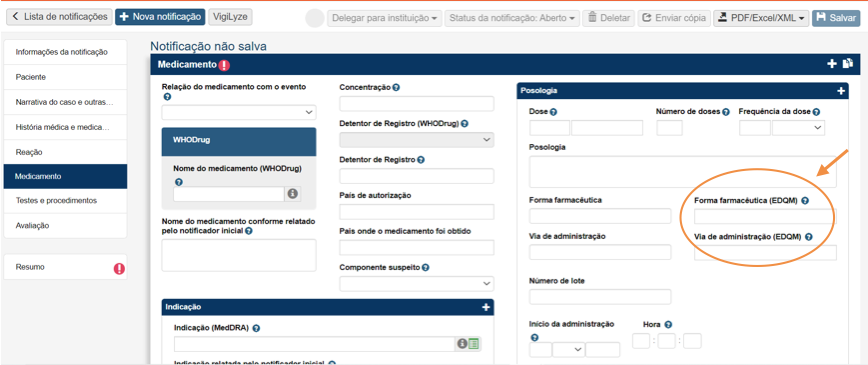
Outra mudança é a incorporação de campos para inclusão dos termos padrão da EDQMrelacionados à forma farmacêutica e via de administração dos medicamentos. No sistemaVigiMed para os serviços de saúde, os notificadores poderão usufruir dessa codificação e priorizar a inclusão da via de administração e forma farmacêutica com esses termos quando forem preencher a aba “Medicamento”.
Para as empresas farmacêuticas, orientações mais detalhadas serão repassadas após a atualização do sistema VigiMed Empresas (eReporting Industry).
Esse importante passo possibilitará à Anvisa recomendar o uso do padrão da EDQM como dicionário para formas farmacêuticas e vias de administração, até que se adquira experiência suficiente para torná-lo obrigatório. A utilização de termos padrão qualifica osdados e imprime mais eficiência ao monitoramento. Em julho de 2020, o Conselho Internacional de Harmonização de Requisitos Técnicos para Produtos Farmacêuticos de Uso Humano – ICH adotou a terminologia Padrão EDQM para formas farmacêuticas e via de administração.
Além desses aprimoramentos, é importante destacar o histórico de medicamentos para o paciente ou progenitor (pai) no VigiMed Serviços de Saúde. Ao preencher qualquer um dos campos do histórico medicamentoso, serão solicitadas informações sobre “medicação anterior”. Anexos do tipo “png” serão aceitos para uploads de arquivos de até 15 MB. Já noVigiMed Empresas, será solucionado o problema de tempo limite, na importação de ICSRs, para arquivos xml ICH E2B (R2 e R3) grandes.
Leia também:
- Realizada 1ª reunião da Câmara Técnica de Farmacovigilância
- VigiMed Empresas: Anvisa anuncia mais avanços no sistema
Fonte: Anvisa, em 17.05.2022.
