Anvisa integra missão brasileira na China
Agenda visa fortalecer a cooperação bilateral com foco na transferência de tecnologia para o Brasil
X
Daniela Marreco, diretora da Anvisa, representa oficialmente a Agência na delegação do governo brasileiro em missão na China - João Risi/Ministério da Saúde
A Agência Nacional de Vigilância Sanitária (Anvisa) integra, até a próxima quinta-feira (19/3), a delegação do governo brasileiro que visita à República Popular da China. A missão tem como objetivo principal o fortalecimento da cooperação bilateral, com foco na transferência de tecnologia para o Brasil.
A diretora Daniela Marreco representa oficialmente a Agência na delegação, que fará visitas a empresas fabricantes de dispositivos médicos, medicamentos, hemoderivados. Além disso, haverá visitas a instituições de saúde, como hospitais inteligentes, e reuniões para tratar de possíveis cooperações entre os dois países.
Veja mais fotos da missão do governo brasileiro à República Popular da China
https://www.flickr.com/photos/203878139@N07/albums/72177720332580538/
Anvisa manda recolher fitas de clareamento dental
Produtos registrados como cosméticos alegavam benefícios terapêuticos no rótulo
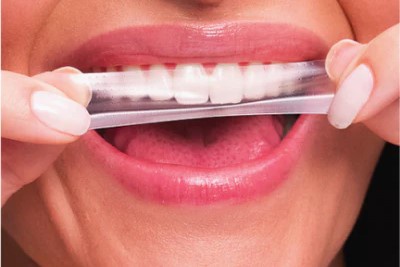
Os produtos estavam sendo comercializados de maneira irregular – Foto: Divulgação
A Agência Nacional de Vigilância Sanitária (Anvisa) publicou, nesta segunda-feira (16/3), uma medida que determina o recolhimento da fita de clareamento Oiwhite, produzida pela empresa Belcher Farmacêutica do Brasil S.A., e a fita Oiwhite – Fita Clareadora Dental Roxa, fabricada pela empresa Endogem Indústria, Comércio, Importação, Exportação, e Serviços LTDA.
A medida proíbe a comercialização, a distribuição, a importação, a propaganda e o uso para os dois produtos. Os dois produtos estavam sendo comercializados de maneira irregular, pois estavam indevidamente regularizados como cosméticos, apesar de fazerem promessas terapêuticas no rótulo, o que é proibido.
Tônico capilar
A informação indevida de alegações terapêuticas na rotulagem também foi o motivo da determinação de recolhimento do tônico capilar Bio Calmante Neo Derma e do Shampoo para Controle de Caspa Neo Dermax, ambos da empresa Through Indústria e Comércio de Cosméticos LTDA.
Os produtos não podem ser comercializados, distribuídos, fabricados, divulgados e utilizados.
Confira as medidas previstas na Resolução 976/2026, publicada no Diário Oficial da União (DOU) desta segunda-feira (16/3).
Guia sobre estudos de preferência de pacientes está em consulta pública
Edital de chamamento abre Consulta Pública Regional sobre o Guia E22 do ICH.
A Agência Nacional de Vigilância Sanitária (Anvisa) publicou o Edital de Chamamento nº 2, de 11 de março de 2026, para coletar contribuições ao Guia E22 do ICH (do inglês International Council for Harmonisation of Technical Requirements for Pharmaceuticals for Human Use – Conselho Internacional de Harmonização de Requisitos Técnicos para Produtos Farmacêuticos de Uso Humano). O documento aborda considerações gerais para estudos de preferência de pacientes (PPS).
O prazo para participação já está aberto e vai até 14/4/2026. As contribuições devem ser feitas em formulário eletrônico específico.
Qualquer interessado no tema abordado pelo guia pode contribuir, em especial patrocinadores de ensaios clínicos, Organizações Representativas de Pesquisa Clínica (ORPCs), equipes de centros de pesquisa, representantes de Comitês de Ética em Pesquisa, professores e pesquisadores da área, demais profissionais e pessoas físicas e jurídicas envolvidas com o desenvolvimento clínico e registro de medicamentos e produtos biológicos.
O texto proposto do guia ICH EWG E22 está disponível no site do ICH, no link.
Para contribuir, é recomendado observar os seguintes pontos:
- Priorizar ou destacar os principais comentários.
- Correlacionar seu comentário com o número da linha correspondente do guia, para facilitar a identificação do texto.
- Fornecer justificativa e quaisquer exemplos relevantes para apoiar as mudanças sugeridas.
- Apresentar sugestão de nova escrita, sempre que possível.
- Consolidar comentários da mesma organização, se apropriado.
- Elaborar o comentário preferencialmente em inglês.
Contextualização
Como membro do ICH, a Anvisa colabora com o processo de discussão e harmonização dos requisitos técnicos para medicamentos em diversos grupos de trabalho (GTs). Dentre eles, a Agência participa do GT referente ao Guia ICH E22 sobre considerações gerais para estudos de preferência de pacientes (PPS).
Estudos de Preferência dos Pacientes (Patient Preference Studies – PPS) têm como objetivo avaliar a desejabilidade ou a aceitabilidade relativa de intervenções em saúde já existentes ou potenciais, bem como de suas características e desfechos. Esses estudos podem gerar informações estruturadas sobre a importância relativa de diferentes características – também chamadas de atributos – consideradas pelos pacientes no momento da tomada de decisão sobre medicamentos.
A compreensão desses insights qualitativos e quantitativos é fundamental para diversas etapas do desenvolvimento de medicamentos, como a identificação de necessidades médicas não atendidas, o desenho de estudos clínicos e a interpretação de seus resultados.
A minuta do guia apresenta diretrizes sobre o uso de ensaios clínicos confirmatórios com desenho adaptativo, destinados a avaliar um tratamento para determinada condição médica no contexto de seu programa de desenvolvimento.
Estudos de preferência do paciente (PPS) estão sendo cada vez mais utilizados para incorporar a voz do paciente no desenvolvimento e na avaliação de medicamentos. O draft do guia ICH E22 estabelece considerações gerais e princípios científicos para o uso, desenho, condução, análise e submissão de PPS, com o objetivo de apoiar a tomada de decisões ao longo de todo o ciclo de vida do medicamento, incluindo o desenvolvimento, as submissões regulatórias, as aprovações e a manutenção dessas aprovações.
O guia fornecerá princípios de alto nível e orientações práticas para:
- Descrever situações em que os PPS podem ser informativos para o desenvolvimento de medicamentos;
- Considerações sobre desenho de estudo e aspectos metodológicos;
- Documentação do estudo;
- Aspectos operacionais e considerações adicionais.
Para mais detalhes relacionados a esse guia, acesse a página de consultas públicas em andamento, no site do ICH.
Anvisa determina o recolhimento de esmalte em gel com substância proibida
Produtos não podem ser vendidos no Brasil

Substância proibida no Brasil motivou a medida – Foto: Divulgação
Uma ação fiscal da Agência Nacional de Vigilância Sanitária (Anvisa), determinou, nesta segunda-feira (16/3), o recolhimento de esmaltes em gel da marca Impala, fabricados pela empresa Laboratório Avamiller de Cosméticos LTDA.
Veja a lista de produtos:
- Plus Gel Esmalte Impala Gel (todos os lotes);
- Esmalte Gel Impala Gel Plus (todos os lotes);
- Gel Plus Impala Esmalte Gel (todos os lotes);
- Esmalte Gel Plus Impala (todos os lotes);
- Top Coat Gel Impala Gel Plus Clear (todos os lotes).
A medida foi tomada após a empresa comunicar sobre o recolhimento voluntário dos produtos que possuem em suas formulações a substância INCI Trimethylbenzoyl Diphenylphosphine Oxide (TPO), substância proibida em cosméticos, produtos de higiene pessoal e perfumes no Brasil.
Em 30 de outubro do ano passado, a Anvisa publicou a Resolução da Diretoria Colegiada (RDC) 995/2025, que alterou o anexo da RDC 529/2021, que dispõe sobre a lista de substâncias que não podem ser utilizadas em produtos de higiene pessoal, cosméticos e perfumes.
Confira a Resolução (RE) 976/2026 no Diário Oficial da União.
Leia também: Anvisa proíbe duas substâncias utilizadas em produtos para unhas
Anvisa determina apreensão de azeite San Olivetto
Origem do produto é desconhecida e importadora está com CNPJ suspenso

A Agência Nacional de Vigilância Sanitária (Anvisa) determinou, nesta segunda-feira (16/3), a apreensão do azeite de oliva extravirgem San Olivetto, da empresa Agro Industria e Cerealista Norte Paraná LTDA. Ficam também proibidos a comercialização, a distribuição, a fabricação, a importação, a propaganda e o uso do produto.
A origem do produto é desconhecida e o rótulo indica como importadora a Agro Indústria e Cerealista Norte Paraná Ltda. A empresa, no entanto, está com CNPJ suspenso por inconsistência cadastral desde 22/5/2025. Já a distribuidora, a empresa Comercial Alimentícia e Cerealista Capixaba Ltda (CNPJ 40.160.646/ 0001-50), está com CNPJ baixado por encerramento desde novembro de 2024.
Confira a Resolução (RE) 986/2026 no Diário Oficial da União.
Fonte: Anvisa, em 16.03.2026.
