Anvisa atualiza alerta sobre ventiladores pulmonares e aparelhos para apneia do sono da Philips
A Anvisa notificou a empresa para apresentar documentação e esclarecimentos técnicos adicionais, que permitam uma melhor avaliação dos riscos à saúde, bem como no que se refere à assistência aos usuários do equipamento
A Anvisa atualizou as informações relacionadas ao acompanhamento das ações de campo da Philips envolvendo alguns modelos de ventiladores pulmonares e aparelhos CPAP (Aparelho de Pressão Positiva Contínua nas Vias Aéreas) e BIPAP (aparelho de Pressão Positiva de Duplo Nível nas Vias Aéreas), onde a espuma de redução de ruído é susceptível à degradação e à emissão de compostos orgânicos voláteis.
O problema
A Philips Respironics iniciou uma ação de campo para os dispositivos descritos acima devido a dois problemas relacionados à espuma de redução de som de poliuretano (PE-PUR) à base de poliéster usada nos ventiladores contínuo e não contínuo da Philips:
1) a espuma PE-PUR pode se degradar em partículas que podem entrar na via de ar do dispositivo e ser ingeridas ou inaladas pelo usuário; e
2) a espuma PE-PUR pode liberar certos produtos químicos.
A degradação da espuma pode ocorrer sob determinadas circunstâncias, influenciadas por fatores que incluem o uso de métodos de limpeza não aprovados, como o ozônio, e determinadas condições ambientais envolvendo altas temperaturas e alto teor de umidade. As condições ambientais, que podem ser uma das causas desse problema, referem-se ao clima e às temperaturas regionais dos países onde os dispositivos são usados e armazenados.
A eliminação de compostos orgânicos voláteis (VOC) presentes na espuma pode ocorrer durante a operação inicial e pode continuar durante toda a vida útil do dispositivo. Os VOC emitidos podem provocar efeitos adversos à saúde a curto e longo prazo. A empresa realizou testes que identificaram dois Compostos de Preocupação (COC) que podem ser emitidos pela espuma e que ultrapassam os limiares de segurança. Os compostos identificados são os seguintes: dimetil diazina e fenol, 2,6-bis (1,1-dimetiletil)-4-(1-metilpropil).
A ausência de partículas visíveis não significa que a desagregação da espuma não esteja ocorrendo. A análise laboratorial da espuma deteriorada revelou a presença de substâncias químicas potencialmente nocivas, incluindo: toluenodiamina; diisocianato de tolueno e dietilenoglicol.
O paciente pode ser exposto a partículas de espuma por inalação ou ingestão, o que pode resultar em dano à saúde. Os possíveis riscos de exposição à espuma deteriorada incluem irritação (na pele, nos olhos e no trato respiratório), resposta inflamatória, dor de cabeça, asma, efeitos adversos em outros órgãos (por exemplo, rins e fígado) e efeitos tóxicos carcinogênicos.
Esses problemas podem resultar em lesões graves, causar comprometimento permanente ou exigir intervenção médica para evitar comprometimento permanente. Foram relatados casos de dor de cabeça, irritação das vias aéreas superiores, tosse, pressão torácica e infecção sinusal.
Não houve relatos de óbito como resultado da exposição às substâncias resultantes da degradação da espuma dos referidos aparelhos.
Em 28 de junho de 2021, a Anvisa proibiu a importação e comercialização dos produtos afetados (RE nº 2.535 de 28 de junho de 2021).
Monitoramento da Anvisa
A Anvisa notificou a empresa para apresentar documentação e esclarecimentos técnicos adicionais, que permitam uma melhor avaliação dos riscos à saúde, bem como no que se refere à assistência aos usuários do equipamento.
Quanto à estratégia de comunicação, foram realizadas reuniões com a Secretaria Nacional do Consumidor (Senacon), do Ministério da Justiça, para entendimento e alinhamento sobre a comunicação de risco aos usuários e suporte da empresa aos clientes.
Além disso, a Anvisa realizou uma consulta internacional quanto ao tema, junto às autoridades reguladoras de outros países como Canadá, Estados Unidos, Japão e comunidade europeia, visando identificar estratégias de avaliação das demais autoridades e presença de sintomatologia relacionado ao uso do produto.
Também está em curso uma consulta junto aos integrantes da rede sentinela e núcleos de segurança do paciente nos serviços hospitalares, com o objetivo de levantar e compreender quaisquer sinais e sintomas relacionados ao uso do equipamento.
Dentro da perspectiva da comunicação de risco, a Anvisa revisou os Alertas 3562 e 3563 trazendo informações técnicas referente à documentação disponibilizada à Agência.
É de responsabilidade da empresa o contato com seus clientes, garantindo a efetividade das ações de reparo ou alternativas de substituição dos equipamentos com problemas.
Para saber mais acesse:
Para acesso ao site da empresa entre em:
https://www.philips.com.br/healthcare/e/sleep/communications/src-update
Divulgados dados do anuário sobre a indústria farmacêutica no Brasil
Organizado pela Secretaria-Executiva da Câmara de Regulação do Mercado de Medicamentos (SCMED), documento traz estatísticas sobre a indústria de fármacos em 2019, além de séries históricas entre 2015 e 2019
A Secretaria-Executiva da Câmara de Regulação do Mercado de Medicamentos (SCMED), unidade administrativa exercida pela Anvisa, acaba de lançar a 5ª edição do Anuário Estatístico do Mercado Farmacêutico. Em uma versão comemorativa, a publicação traz dois grandes recortes de informações: um dedicado ao panorama do mercado em 2019 e outro com séries históricas entre 2015 e 2019.
O objetivo do anuário é oferecer, de forma racional e organizada, estatísticas sobre a indústria de fármacos no Brasil. Para traçar o perfil do mercado, o levantamento considerou dados consolidados até julho de 2020 sobre produtos farmacêuticos regulados pela Câmara de Regulação do Mercado de Medicamentos (CMED), divididos em seis grupos distintos de fármacos: biológicos, específicos, genéricos, similares, novos e fitoterápicos.
Portanto, a publicação traz uma série de recortes, com uma ampla gama de informações sobre a indústria, o faturamento obtido no ano, produtos comercializados, características dos medicamentos, canais de distribuição, substâncias mais comercializadas e vários outros recortes.
O documento usa informações do Sistema de Acompanhamento do Mercado de Medicamentos (Sammed).
Dados gerais
De acordo com as informações do anuário, a venda de medicamentos no Brasil gerou um faturamento de R$ 85,9 bilhões em 2019. Em termos percentuais, o valor da comercialização refletiu um crescimento de 7,9% em relação a 2018. Quanto à quantidade de embalagens, o aumento foi de 15,4% de um ano para o outro, passando de 4,6 bilhões para 5,3 bilhões.
O relatório revela também que, em 2019, foram identificados 5.897 produtos cadastrados e em comercialização no país. Destes, 40,4% eram medicamentos similares e 39,6%, genéricos. Portanto, similares e genéricos corresponderam a 80% dos produtos cadastrados e em comercialização. Outros tipos de produtos representaram 33,8%.
O documento aponta que o faturamento dos medicamentos novos apresentou maior representatividade no mercado, somando mais de R$ 30,5 bilhões, seguido do valor da categoria de biológicos (R$ 21,8 bilhões) e de similares (R$ 17,2 bilhões).
Preços médios
O anuário destaca que o preço médio global de medicamentos praticado em 2019 foi de R$ 16,34. Os fármacos similares tiveram mediana de R$ 9,22. Na sequência, ficaram os medicamentos biológicos, com preço médio praticado de R$ 133,44. Já os medicamentos genéricos apresentaram preço médio de R$ 6,35. Na outra ponta, ficaram os medicamentos para tratamento de cânceres (R$ 595,80).
Embalagens
De acordo com a publicação, os medicamentos similares tiveram a maior quantidade de embalagens comercializadas, atingindo cerca de 1,9 bilhão de unidades, ou 35,5% do total. Os genéricos vêm na sequência, com 1,8 bilhão de embalagens comercializadas em 2019 (35,2%). Juntos, similares e genéricos somaram 3,7 bilhões de embalagens, representando 70,7% das unidades comercializadas naquele ano.
Empresas, apresentações e princípios ativos
Segundo as informações do documento, o número de empresas que comercializaram medicamentos no Brasil passou de 221, em 2018, para 224, em 2019. Juntas, essas empresas venderam 13.888 apresentações de medicamentos, 4,3% a mais do que em 2018.
Conforme a publicação, o termo “apresentação” refere-se ao Código Nacional de Produtos (CNP), que contém, por exemplo, informações sobre concentração do princípio ativo, forma farmacêutica e embalagem. Portanto, é um dado referente à rotulagem do produto.
Com relação à quantidade de princípios ativos, matérias-primas envolvidas na produção de medicamentos, foram identificadas um total de 1.935. O anuário informa também um crescimento de 5% (de 478 para 502) na quantidade de subclasses terapêuticas existentes no mercado brasileiro de medicamentos, entre 2018 e 2019. Essas subclasses representam subdivisões de classes terapêuticas, ou seja, de tratamentos, conforme a ação do medicamento no organismo.
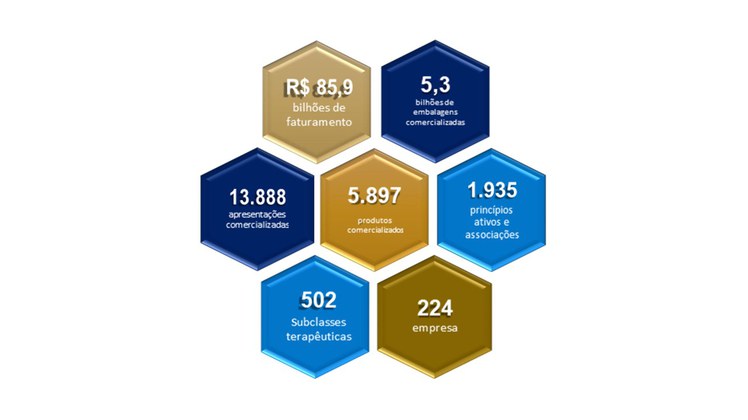
Confira abaixo um resumo do panorama geral do mercado farmacêutico em 2019.
Leia a íntegra da 5ª edição do Anuário Estatístico do Mercado Farmacêutico, com dados de 2019 e séries históricas de 2015 a 2019.
Vacinação contra Covid-19: a importância da segunda dose
Sua imunização só estará completa com a dose de reforço. Na data marcada, compareça ao local de vacinação
Chegou o dia de tomar a segunda dose? Não perca tempo! Complete a imunização e preserve sua saúde. É importante tomar a dose de reforço da vacina contra Covid-19, quando existe a previsão, porque a eficácia do imunizante foi comprovada a partir de análises realizadas com as duas aplicações.
A pessoa que não completa o esquema vacinal fica mais vulnerável à infecção pelo novo coronavírus (Sars-CoV-2) do que aquela que recebeu as duas doses. Ou seja, além de se expor ao risco de ser contaminado e adoecer, esse indivíduo não ajuda a controlar a circulação do vírus. E tem mais: a vacinação incompleta pode criar um ambiente propício para o surgimento de versões ainda mais resistentes do coronavírus.
Imagine a seguinte situação: há invasores à solta que procuram hospedagem nos organismos. Alguns organismos, por razões ainda desconhecidas, conseguem expulsá-los com tranquilidade. Outros lutam por horas, dias ou meses e conseguem vencer a batalha. Há também quem lute de forma aguerrida e perca a vida.
A vacina, portanto, entra em cena para torná-lo mais resistente ao ataque desses vírus invasores! Se uma determinada vacina prevê duas aplicações, isso significa que as duas doses são necessárias para fortalecer seu sistema imunológico, deixando-o mais preparado para enfrentar um possível combate.
De acordo com o diretor-presidente da Anvisa, Antonio Barra Torres, as vacinas são, neste momento, a medida farmacológica de maior comprovação, credibilidade e eficácia disponível em todo o mundo. “Não faz sentido a pessoa tomar uma dose da vacina e não se apresentar para tomar a segunda dose. Quem assim o faz está com uma proteção insuficiente e inadequada”, alerta.
Passou do prazo?
Se você se lembrou da data de retorno ou mudou de ideia sobre a importância da nova dose e perdeu o prazo, vale o dito popular “antes tarde do que nunca”. Mesmo fora do prazo, é absolutamente relevante concluir o esquema vacinal. Completar esse esquema não quer dizer reiniciar a contagem e tomar a primeira dose do imunizante novamente. Basta tomar a segunda dose e seguir a vida, tomando os cuidados necessários até que a vacina chegue no braço de todos.
Ah, se você tomou a primeira dose e sentiu desconfortos leves, entenda que esses sintomas são passageiros e não devem ser motivo para abrir mão da segunda dose da vacina contra Covid-19. Para se alcançar a imunidade coletiva, que pode frear a transmissão do vírus e fazer com que todos retomemos mais rapidamente a normalidade, é preciso que cerca de 70% da população complete o ciclo vacinal. O Brasil necessita alcançar esse patamar de imunidade coletiva para ver e viver o efeito esperado da vacinação. Para isso, cada um precisa fazer a sua parte.
Vá ao local de vacinação e tome a segunda dose quando chegar a hora! Faça isso por você, pelos seus familiares, pelos seus amigos e por uma sociedade mais saudável!
Edital de Chamamento trata sobre o Guia ICH S12
Está aberto até o dia 6 de setembro o prazo para enviar contribuições para o Guia S12 de Estudos Não Clínicos de Biodistribuição para o Desenvolvimento de Produtos de Terapia Gênica!
A Anvisa informa que já está aberto o prazo para contribuição do Edital de Chamamento Público 11/2021, que trata do Guia S12 de Estudos Não Clínicos de Biodistribuição (BD) para o Desenvolvimento de Produtos de Terapia Gênica (Guideline S12 on Nonclinical Biodistribution Considerations for Gene Therapy Products) do Conselho Internacional de Harmonização (ICH).
Os interessados poderão enviar suas contribuições até o dia 6 de setembro deste ano, por meio de formulário eletrônico. O referido edital foi publicado no Diário Oficial da União (D.O.U.) do dia 9 de julho, com prazo de 60 dias para participação.
É importante esclarecer que o guia tem como objetivo proporcionar recomendações harmonizadas para a condução desses estudos. O documento apresenta diretrizes como o desenho de ensaios de biodistribuição, além de considerações sobre interpretações e aplicações, de forma a dar suporte ao desenvolvimento não clínico e clínico de produtos de terapias gênicas.
Além disso, a publicação visa minimizar o uso desnecessário de animais em ensaios não clínicos. Por fim, destaca-se que a perspectiva é que o guia seja utilizado no Brasil como documento de apoio ao processo de regularização de ensaios clínicos com produtos de terapia gênica em desenvolvimento no país.
Clique aqui e envie a sua contribuição!
Fonte: Anvisa, em 13.07.2021
