O protocolo foi recebido nesta sexta-feira (13/5) e já está em avaliação pelas áreas técnicas envolvidas. O prazo de análise da Agência é de 60 dias.
A Anvisa recebeu o pedido de registro da vacina Convidecia, contra a Covid-19. A solicitação foi apresentada pela empresa farmacêutica Biomm SA, que representa no Brasil o fabricante do imunizante, a CanSino Biologicals .
A vacina utiliza a tecnologia de adenovírus vetor, semelhante a de outras vacinas já em uso no país e o pedido para uso em adultos.
O pedido foi apresentado à Anvisa no âmbito da RDC 415/2020, que traz critérios e procedimentos extraordinários para pedidos de registro decorrentes do novo Coronavírus. A norma prevê, por exemplo, a análise prioritária e a possibilidade de se firmar termos de compromisso, como foi feito com outras vacinas contra Covid-19 já autorizadas no Brasil.
O protocolo foi recebido nesta sexta-feira (13/5) e já está em avaliação pelas áreas técnicas envolvidas. O prazo de análise da Agência é de 60 dias.
Processo de análise
A análise de vacinas pela Anvisa é feita de forma conjunta por três áreas distintas:
- a área de Medicamentos, que avalia os aspectos de segurança e eficácia;
- a área de Farmacovigilância, responsável pelo monitoramento e planos de acompanhamento da vacina após sua entrada em uso no país; e
- a área de Inspeção e Fiscalização, responsável pela avaliação das Boas Práticas de Fabricação.
Anvisa faz reunião com Butantan sobre CoronaVac para crianças
A atividade é parte do processo de solicitação de indicação da vacina para crianças de 3 a 5 anos.
A Anvisa realizou nesta sexta-feira (13/5) reunião com o Instituto Butantan sobre uso da vacina CoronaVac para crianças. A atividade é parte do processo de solicitação de indicação da vacina para crianças de 3 a 5 anos.
Na última terça-feira (10/5) o Instituto enviou para a Anvisa dados e informações em resposta ao pedido de exigência feito pela Anvisa para suprir lacunas no processo. Estes dados ainda estão em análise pela equipe técnica da Anvisa.
A resposta recebida pela Anvisa, no entanto, ainda não contempla todos os itens indicados pela equipe técnica no pedido de exigência.
De acordo com o Butantan, as informações restantes, que são os dados atualizados de estudos de efetividade feitos no Chile, ainda serão enviados para a Agência. Segundo o laboratório, os dados já foram solicitados aos pesquisadores daquele país e serão compartilhados com a Anvisa.
A Anvisa também reiterou em 06/05/20022, o ofício já enviado ao Chile, no qual a Agência reafirma a importância de manter a parceria, e troca de informações a respeito dos estudos que estão sendo conduzidos com a vacina CoronaVac., em especial, quanto ao estudo de efetividade das vacinas aplicadas em crianças Chile.
Por fim, a Anvisa mantém o seu compromisso na avaliação da vacinas, balizando as suas ações dentro da legalidade, dos parâmetros estabelecidos em suas normativas, convergentes com as principais autoridades estrangeiras e com os ditames científicos.
Realizada 1ª reunião da Câmara Técnica de Farmacovigilância
Os membros da Câmara Técnica aprovaram a criação de dois grupos de trabalho. Leia a matéria e fique por dentro dos avanços.
A Anvisa informa que, na última quinta-feira (12/5), foi realizada a primeira reunião da Câmara Técnica de Farmacovigilância, a CTFARM, com a formação internacional instituída pela Portaria 222/2022. Durante o encontro, os novos membros aprovaram a criação de dois grupos de trabalho e tiveram a oportunidade de conhecer melhor os aspectos regulatórios do mercado brasileiro de medicamentos e os marcos históricos da farmacovigilância no Brasil.
Um dos novos grupos de trabalho irá tratar da formalização do Sistema Nacional de Farmacovigilância, pauta da Agenda Regulatória da Anvisa 2022-2023. O outro grupo irá avaliar a definição do método para análise dos relatórios de avaliação benefício-risco de medicamentos, a fim de ampliar o conhecimento e agilizar a detecção de sinais de segurança, para aprimoramento do processo decisório quanto à vigilância pós-mercado de medicamentos no Brasil. Ambos têm objetivos claros a serem alcançados em curto e médio prazos.
Essa primeira reunião contou com a participação dos membros titulares e suplentes da CTFARM e de servidores da Agência, que estiveram presentes como convidados.
Entenda
A Câmara Técnica contribuirá para a realização de benchmarking, ou seja, de uma análise mais minuciosa das melhores práticas, com experiências de outros países. Os membros da CTFARM também irão compor os grupos de trabalho com os convidados especializados nos temas.
Oportunidade
A Anvisa publicou a Carta de Manifestação de Interesse 1/2022 para projetos que têm como objetivo incentivar o fortalecimento e a modernização do ensino, da pesquisa e do desenvolvimento das ações de farmacovigilância no país.
O prazo para envio de projetos vai até 20 de maio. A ação é voltada a instituições públicas de ensino superior, credenciadas junto ao Ministério da Educação (MEC), que ofereçam cursos de graduação em saúde e desenvolvam atividades de ensino, pesquisa e extensão.
Leia também:
Anvisa investe no fortalecimento e na modernização da farmacovigilância
Fitoterápicos da Farmacopeia Brasileira: aberta consulta pública
Objetivo é atualizar o texto da monografia da Maytenus ilicifolia Mart. ex Reissek. Prazo para contribuições termina em 24/6.
Está aberto o prazo para envio de contribuições à Consulta Pública (CP) 1.093/2022, que propõe a atualização do texto da Maytenus ilicifolia Mart. ex Reissek. do Formulário de Fitoterápicos da Farmacopeia Brasileira 2ª edição, de que trata a Resolução da Diretoria Colegiada (RDC) 463/2021.
Os interessados têm até o dia 24 de junho para enviar suas contribuições, por meio de formulário específico disponibilizado pela Anvisa. A proposta dessa consulta foi elaborada pelo Comitê Técnico Temático de Plantas Medicinais da Farmacopeia Brasileira. A revisão da monografia visa a elaboração de novas formulações em substituição à antiga Formulação nº 2 (cápsula com derivado), em vias de ser excluída pela RDC 678/2022. Mais informações sobre a exclusão da Formulação nº 2 podem ser encontradas no Voto 53/2002, que subsidiou a aprovação da RDC 678/2022.
Sobre a Consulta Pública
As sugestões à Consulta Pública (CP) 1.093/2022 devem ser enviadas por meio de um formulário eletrônico específico. As contribuições recebidas, exceto os dados pessoais informados pelos participantes, são consideradas públicas e de livre acesso.
Após o preenchimento do formulário eletrônico será disponibilizado um número de protocolo ao participante, sendo dispensado o envio postal ou protocolo presencial de documentos em meio físico junto à Anvisa.
Em caso de limitação de acesso do cidadão à internet, será permitido o envio de sugestões por escrito, em meio físico, durante o prazo da consulta, para o seguinte endereço: Anvisa/Coordenação da Farmacopeia – SIA, Trecho 5, Área Especial 57 – Brasília-DF – CEP 71.205-050. Contribuições internacionais, excepcionalmente, poderão ser encaminhadas em meio físico, para o mesmo endereço, aos cuidados da Assessoria de Assuntos Internacionais (Ainte).
Encerrado o prazo da CP, a Anvisa analisará as contribuições e, ao final, publicará o resultado aqui, no portal da Agência. Se houver necessidade, a Agência poderá se articular com órgãos e entidades envolvidos com o assunto, bem como com aqueles que tenham manifestado interesse na matéria, para subsidiar posteriores discussões técnicas e a deliberação final da Diretoria Colegiada.
Participe da Consulta Pública (CP) 1.093/2022.
Plano de Transformação Digital da Anvisa 2021-2022 é repactuado
Medida reafirma o compromisso da Agência com a estratégia do Governo Digital, para aumentar a eficiência e melhorar os serviços prestados à sociedade.
AAnvisa informa que renovou a parceria com a Secretaria de Governo Digital (SGD/ME) e com a Secretaria Especial de Modernização do Estado (Seme/SG-PR), mediante a repactuação do Plano de Transformação Digital da Agência para o período 2021-2022. A iniciativa ocorreu em conjunto com o Ministério da Economia e a Presidência da República.
O objetivo da medida é dar continuidade à transformação de serviços da Anvisa, bem como aumentar a maturidade digital daqueles já disponibilizados no portal da instituição. Até o final deste ano, a Agência pretende realizar a transformação digital de 88 dos seus serviços de atendimento ao usuário. Isso representa um aumento de 67% para 90% dos serviços digitais prestados pela Agência.
Nesse sentido, é importante lembrar que, em 2019, esse percentual era de 19%. Ressalta-se ainda que faz parte da meta aumentar o nível de maturidade digital de oito serviços já digitalizados.
Veja os objetivos específicos do Plano de Transformação Digital:
- Ampliar a oferta de serviços digitais para o cidadão.
- Propiciar maior autonomia, transparência e satisfação aos usuários.
- Desburocratizar os serviços prestados pela Agência, chegando-se ao mínimo de burocracia viável para alcançar os objetivos do interesse público.
- Reduzir o tempo médio de atendimento e o custo na prestação dos serviços.
- Promover a integração e o uso de inteligência de dados na prestação dos serviços.
- Promover a segurança e a disponibilidade dos serviços ofertados, bem como proteger a privacidade do cidadão.
Vinculação do projeto e-Notivisa ao Startup Gov.br
Um dos destaques da repactuação foi a inclusão do e-Notivisa como projeto vinculado ao programa Startup Gov.br, liderado pelo Ministério da Economia. A aprovação desse projeto nesse rol representa uma grande conquista para a Anvisa.
O e-Notivisa tem os seguintes objetivos: melhorar a experiência dos usuários do sistema de notificação, como agentes participativos; modernizar a plataforma, estimulando e ordenando a participação dos agentes envolvidos em toda a cadeia pós-uso; e simplificar e agilizar a atuação dos setores produtivos e comerciais, órgãos e instituições oficiais e estabelecimentos de saúde direta ou indiretamente envolvidos com produtos regulados.
Além disso, o projeto visa promover a integração do processo de monitoramento do Vigipós (sistema de vigilância pós-comercialização/pós-uso), agregando conceitos de trabalho em rede, inteligência artificial, mineração de dados e algoritmos de risco para prospecção de dados, de modo a assegurar resultados e verificações mais diligentes e precisas.
Saiba mais
Entre 2019 e 2021, a Anvisa transformou 204 serviços oferecidos à sociedade, tendo sido o órgão do governo federal que mais contribuiu para a digitalização de serviços pela segunda vez consecutiva, conforme levantamento da SGD/ME.
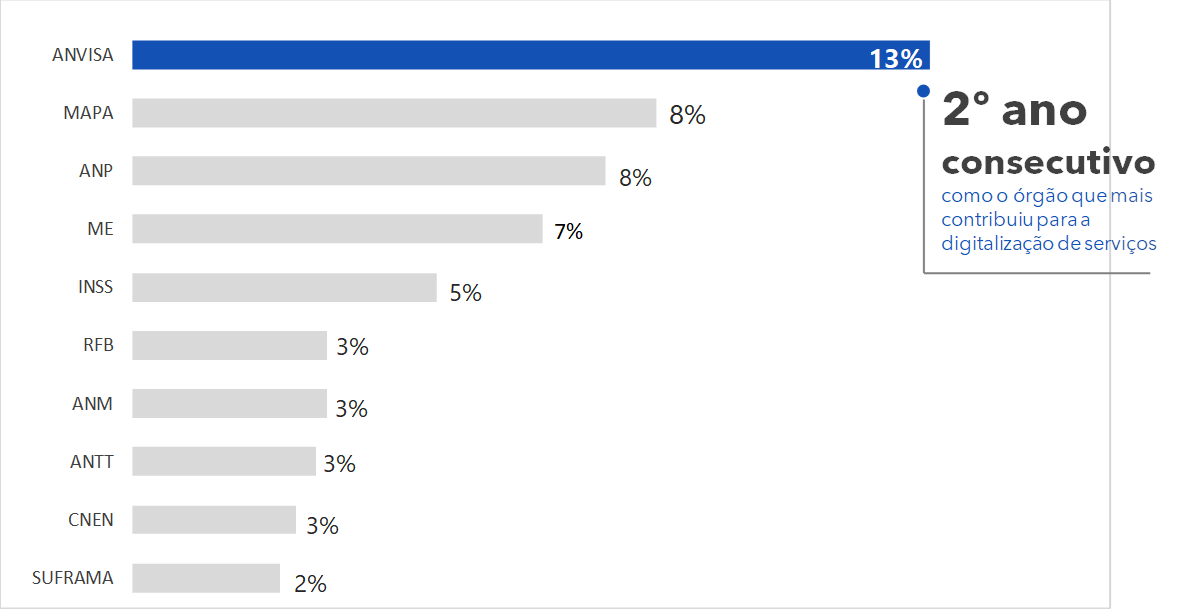
Esta posição foi elogiada pela SGD e pela Seme, que, durante a reunião de repactuação, destacaram o papel de vanguarda desempenhado pela Agência dentre os órgãos federais. Após a aprovação da repactuação do Plano de Transformação Digital da Anvisa pelo Comitê Estratégico, composto pela Anvisa, pela SGD e pela Seme, o plano foi aprovado pela Diretoria Colegiada da Agência, conforme previsto na Nova Política de Governança Organizacional da Anvisa, instituída pela Portaria 60/2022.
Controle da infecção hospitalar: prevenção é fundamental
Para celebrar o Dia de Prevenção das Infecções Hospitalares, Anvisa e parceiros promovem campanha sobre prevenção de infecções cirúrgicas.
O Dia Nacional de Prevenção das Infecções Hospitalares, celebrado todos os anos no dia 15 de maio, visa conscientizar as autoridades sanitárias, gestores de hospitais e trabalhadores da saúde sobre a importância do controle das infecções hospitalares. Neste ano, a Anvisa e parceiros (*) promovem a campanha nacional “Cirurgias seguras: prevenção de infecções de sítio cirúrgico”.
Com a retomada das cirurgias represadas durante a pandemia de Covid-19, é ainda mais relevante conscientizar os gestores e os profissionais da saúde, bem como a população, sobre a necessidade de implementar ações de prevenção e controle das infecções cirúrgicas.
(*) Associação Brasileira dos Profissionais em Controle de Infecções e Epidemiologia Hospitalar (ABIH), Colégio Brasileiro de Cirurgiões (CBC) e Projeto Prevcovid-BR (coordenado pela Escola de Enfermagem da USP, com apoio técnico do Centro de Controle e Prevenção de Doenças dos Estados Unidos – CDC/EUA)
Cirurgia seguras
O que deve ser feito para uma cirurgia segura e para que não ocorram infecções associadas às cirurgias:
- Higiene adequada das mãos pelos profissionais de saúde, seguindo a técnica correta, seja na antissepsia ou preparo pré-operatório das mãos com água, seja na antissepsia cirúrgica das mãos com produto à base de álcool.
- Antibioticoprofilaxia: inclui a escolha do medicamento adequado, levando em consideração o sítio a ser operado; a administração da dose efetiva em até 60 minutos antes da incisão cirúrgica; atenção especial em relação ao uso de torniquetes (administração da dose total antes de insuflar o torniquete); descontinuação da dose em, no máximo, 24 horas; ajuste da dose em pacientes obesos; repetição das doses em cirurgias prolongadas; e combinação da administração via intravenosa (IV) e via oral (VO) de antimicrobianos para cirurgia colorretal.
- Tricotomia: a retirada dos pelos só deverá ocorrer quando estritamente necessária, de acordo com a área na qual será feita a cirurgia, utilizando-se um tricotomizador.
- Controle de glicemia no pré-operatório e no pós-operatório imediato.
- Manutenção da normotermia (temperatura considerada normal do corpo humano) em todo o perioperatório, ou seja, em todo o tempo relacionado ao ato cirúrgico.
- Utilização de antissépticos que contenham álcool, associados a clorexedina ou iodo, no preparo da pele do paciente antes da cirurgia.
- Emprego da Lista de Verificação de Segurança Cirúrgica (LVSC) para evitar a ocorrência de danos ao paciente.
- Realização de vigilância de casos de infecção por busca ativa.
- Orientação a pacientes e familiares sobre as principais medidas de prevenção de infecção do sítio cirúrgico, como a higiene das mãos e cuidados com curativos e drenos.
Participe da campanha!
Durante esses dias, e não somente em 15 de maio, os serviços de saúde são convidados a desenvolver campanhas de comunicação social e ações educativas, com o objetivo de aumentar a consciência pública sobre o problema representado pelas infecções hospitalares e a necessidade de seu controle.
A fim de reforçar as principais medidas que devem ser adotadas para a prevenção das infecções cirúrgicas, a Anvisa promoverá um seminário virtual sobre o tema no dia 16/5, às 10h, com o Dr. Luiz Carlos Von Bahten, do Colégio Brasileiro de Cirurgiões, e com a Dra. Viviane Maria de Carvalho Hessel Dias, presidente da Associação Brasileira dos Profissionais em Controle de Infecção e Epidemiologia Hospitalar. Os interessados deverão acessar, no dia e hora marcados, o link https://bit.ly/36rmdTS.
Fonte: Anvisa, em 13.05.2022.
