Nota Anvisa: aplicação de vacinas em crianças com 12 anos ou mais
Somente a Pfizer solicitou a inclusão em bula da indicação da vacina para esta faixa etária
A Anvisa informa que, até o momento, somente a Pfizer solicitou a inclusão em bula da indicação da vacina para crianças com 12 anos ou mais. Esse pedido já foi autorizado pela Anvisa e indicação para esta faixa etária incluída na bula da vacina Comirnaty.
Não há solicitação do Instituto Butantan para alteração de bula da CoronaVac e inclusão de crianças e adolescentes. Portanto, não há pedido dependendo de análise da Anvisa.
A competência para solicitar a inclusão de novas indicações na bula é do laboratório que deve ser fundamentada em estudos que sustentem a indicação pretendida tanto em relação aos aspectos de segurança como de eficácia.
Desde o início do ano passado a Anvisa tem realizado um troca de informações frequentes com os laboratórios envolvidos no desenvolvimento de vacinas contra Covid, assim como tem acompanhado todas as publicações científicas sobre o tema. Porém não há pedido de aprovação da CoronaVac para esta faixa etária.
A decisão sobre o registro e alterações no pós-registro de uma vacina ou medicamento é da área técnica. Para as vacinas em uso emergencial esta decisão é da Diretoria Colegiada.
Anvisa solicita alteração na bula das vacinas da Janssen e da Astrazeneca
Evento adverso raro leva a alteração na bula para incluir contraindicação de uso nas vacinas contra a Covid-19
Na última sexta-feira (9/7), após monitoramento do perfil de eventos adversos esperados com estas vacinas, no Brasil e no mundo, a Anvisa solicitou aos fabricantes Janssen e Astrazeneca/Fiocruz a inclusão na bula da contraindicação de uso para as pessoas com histórico da Síndrome de Extravasamento Capilar.
Na Europa, os casos avaliados pela European Medicines Agency (EMA) também apresentavam histórico familiar de Síndrome de Extravasamento Capilar.
Trata-se de evento adverso raro, mas potencialmente grave. A Anvisa já recebeu relato de uma suspeita de síndrome após vacinação e está avaliando o caso.
Os profissionais de saúde devem estar atentos aos sinais e sintomas da síndrome de vazamento capilar e do risco de recorrência em pessoas que já foram diagnosticadas com a doença.
As pessoas que foram vacinadas com plataforma adenoviral devem procurar assistência médica imediata se sentirem inchaço rápido dos braços e pernas ou aumento repentino de peso nos dias seguintes a vacinação. Estes sintomas estão frequentemente associados à sensação de desmaio (devido à pressão arterial baixa).
A síndrome
A síndrome de vazamento capilar é uma condição muito rara e grave que causa vazamento de fluido de pequenos vasos sanguíneos (capilares), resultando em inchaço principalmente nos braços e pernas, baixa pressão arterial, espessamento do sangue e baixos níveis de albumina no sangue (uma importante proteína do sangue).
Torna-se necessário que os cidadãos e profissionais de saúde fiquem atentos aos sinais e sintomas do evento adverso e notifiquem imediatamente os casos suspeitos. É imprescindível o cuidado na identificação do tipo de vacina envolvida na suspeita, como número do lote e fabricante.
Notificação
A notificação de casos suspeitos de eventos adversos relacionados a miocardite ou pericardite poderá ser registrada por meio do sistema VigiMed, Notivisa e e-SUS Notifica.
Medicamentos sintéticos: novos códigos para petição
Novos códigos de assuntos para petição secundária de registro e pós-registro já estão disponíveis, bem como materiais sobre o tema
A Anvisa informa que os novos códigos de assuntos para petição secundária de registro e pós-registro de medicamentos sintéticos já estão disponíveis. Portanto, os códigos antigos serão excluídos do sistema de peticionamento eletrônico.
Também já foram disponibilizados os documentos do seminário virtual realizado em 5/7 sobre o novo fluxo de publicação para medicamentos sintéticos, inclusive o texto que reúne as principais perguntas e respostas sobre o tema. Os materiais estão reunidos neste link. É importante observar que as perguntas e respostas serão atualizadas periodicamente. O recebimento de contribuições pode ser realizado por meio de formulário específico.
Confira abaixo as alterações:
Registro:
|
Códigos antigos |
Códigos novos |
|
11627 GENÉRICO – Formulário de informações relativas à documentação de registro (FIDR) ou Parecer de Análise Técnica da Empresa (Pate) |
12107 GENÉRICO – Formulário de informações relativas à documentação de registro (FIDR) – Análise de Qualidade Registro |
|
11626 MEDICAMENTO INOVADOR – Formulário de informações relativas à documentação de registro (FIDR) ou Parecer de Análise Técnica da Empresa (Pate) |
12108 MEDICAMENTO INOVADOR – Formulário de informações relativas à documentação de registro (FIDR) – Análise de Qualidade Registro |
|
11625 MEDICAMENTO NOVO –Formulário de informações relativas à documentação de registro (FIDR) ou Parecer de Análise Técnica da Empresa (Pate) |
12109 MEDICAMENTO NOVO – Formulário de informações relativas à documentação de registro (FIDR) – Análise de Qualidade Registro |
|
11628 SIMILAR – Formulário de informações relativas à documentação de registro (FIDR) ou Parecer de Análise Técnica da Empresa (Pate) |
12110 SIMILAR – Formulário de informações relativas à documentação de registro (FIDR) – Análise de Qualidade Registro |
Pós-registro:
|
Códigos antigos |
Códigos novos |
|
11627 GENÉRICO – Formulário de informações relativas à documentação de registro (FIDR) ou Parecer de Análise Técnica da Empresa (Pate) |
12111 GENÉRICO – Parecer de Análise Técnica da Empresa (Pate) – Análise de qualidade Pós-Registro |
|
11626 MEDICAMENTO INOVADOR – Formulário de informações relativas à documentação de registro (FIDR) ou Parecer de Análise Técnica da Empresa (Pate) |
12112 MEDICAMENTO INOVADOR – Parecer de Análise Técnica da Empresa (Pate) – Análise de qualidade Pós-Registro |
|
11625 MEDICAMENTO NOVO – Formulário de informações relativas à documentação de registro (FIDR) ou Parecer de Análise Técnica da Empresa (Pate) |
12113 MEDICAMENTO NOVO – Parecer de Análise Técnica da Empresa (Pate) – Análise de qualidade Pós-Registro |
|
11628 SIMILAR – Formulário de informações relativas à documentação de registro (FIDR) ou Parecer de Análise Técnica da Empresa (Pate) |
12114 SIMILAR – Parecer de Análise Técnica da Empresa (Pate) – Análise de qualidade Pós-Registro |
Relatório aponta aumento de 7,9% no faturamento do mercado de medicamentos
Total de vendas chegou a R$ 85,9 bilhões em 2019, com a comercialização de aproximadamente 5,3 bilhões de embalagens de fármacos
A venda de medicamentos no Brasil gerou um faturamento de R$ 85,9 bilhões para a indústria farmacêutica no país em 2019. Em termos percentuais, o valor da comercialização refletiu um crescimento de 7,9% em relação a 2018, quando a indústria faturou R$ 79,6 bilhões. Quanto à quantidade de embalagens, o aumento foi de 15,4% de um ano para o outro, passando de 4,6 bilhões para 5,3 bilhões.
Em 2019, foram identificados 5.897 produtos cadastrados e em comercialização no país – um crescimento de 5,3% em relação a 2018. Destes, 40,4% eram medicamentos similares e 39,6%, genéricos. Portanto, similares e genéricos corresponderam a 80% dos produtos cadastrados e em comercialização naquele ano. Os outros tipos de produtos representaram 33,8% do total.
O faturamento dos medicamentos novos apresentou maior representatividade no mercado, somando mais de R$ 30,5 bilhões, seguido da categoria de biológicos, que acumulou R$ 21,8 bilhões. Em terceiro lugar ficaram os medicamentos similares, com faturamento de R$ 17,2 bilhões.
Publicação
Os dados são do Anuário Estatístico do Mercado Farmacêutico, que chega à sua 5ª edição em uma versão comemorativa, trazendo dois grandes recortes de informações: um dedicado ao panorama do mercado em 2019 e outro com séries históricas entre 2015 e 2019.
O documento usa informações do Sistema de Acompanhamento do Mercado de Medicamentos (Sammed) e é produzido pela Secretaria-Executiva da Câmara de Regulação do Mercado de Medicamentos (SCMED), unidade administrativa exercida pela Anvisa.
O objetivo é oferecer, de forma racional e organizada, estatísticas sobre a indústria de fármacos no Brasil. Para traçar o perfil do mercado, o levantamento considerou dados consolidados até julho de 2020 sobre produtos farmacêuticos regulados pela Câmara de Regulação do Mercado de Medicamentos (CMED), divididos em seis grupos distintos de fármacos: biológicos, específicos, genéricos, similares, novos e fitoterápicos.
Preços médios
O anuário destaca que o preço médio global de medicamentos praticado em 2019 foi de R$ 16,34. Os fármacos similares tiveram mediana de R$ 9,22 em 2019 – maior queda de preço médio entre 2018 e 2019 (-25,2%). Na sequência, ficaram os medicamentos biológicos, que apresentaram redução de 15,8% entre 2018 e 2019, com preço médio praticado de R$ 133,44.
Embora pequena, vale registrar que os medicamentos genéricos também tiveram queda de 1,7%, fechando o ano de 2019 com o menor preço médio do mercado (R$ 6,35). Na outra ponta, ficaram os medicamentos para tratamento de câncer, com preço médio praticado de R$ 595,80.
Acesse os detalhes sobre preços dos medicamentos na 5ª edição do Anuário Estatístico do Mercado Farmacêutico.
Campeões de vendas
Os medicamentos similares tiveram a maior quantidade de embalagens comercializadas, atingindo o volume de cerca de 1,9 bilhão de unidades, ou 35,5% do total – um crescimento de 35,7% em relação a 2018. Os genéricos vêm na sequência, com 1,8 bilhão de embalagens comercializadas em 2019 (35,2% do total), representando um aumento de 5,9% em relação ao ano anterior. Juntos, portanto, similares e genéricos somaram 3,7 bilhões de embalagens, representando 70,7% das unidades comercializadas em 2019.
Empresas, apresentações e princípios ativos
De acordo com o anuário, o número de empresas que comercializaram medicamentos no Brasil passou de 221, em 2018, para 224, em 2019, o que significou um crescimento de 1,4%. Juntas, essas empresas venderam 13.888 apresentações de medicamentos, 4,3% a mais do que em 2018.
Conforme a publicação, o termo “apresentação” refere-se ao Código Nacional de Produtos (CNP), que contém, por exemplo, informações sobre concentração do princípio ativo, forma farmacêutica e embalagem. Portanto, é um dado referente à rotulagem do produto.
Com relação à quantidade de princípios ativos, que são as matérias-primas envolvidas na produção de medicamentos, houve aumento de 5,9% em 2019, chegando a 1.935 – em 2018, o número ficou em 1.827.
O anuário informa também que, entre 2018 e 2019, houve um crescimento de 5% (de 478 para 502) na quantidade de subclasses terapêuticas existentes no mercado brasileiro de medicamentos. Essas subclasses representam subdivisões de classes terapêuticas, ou seja, de tratamentos, conforme a ação do medicamento no organismo.
Confira abaixo um resumo do panorama geral do mercado farmacêutico no Brasil em 2019.
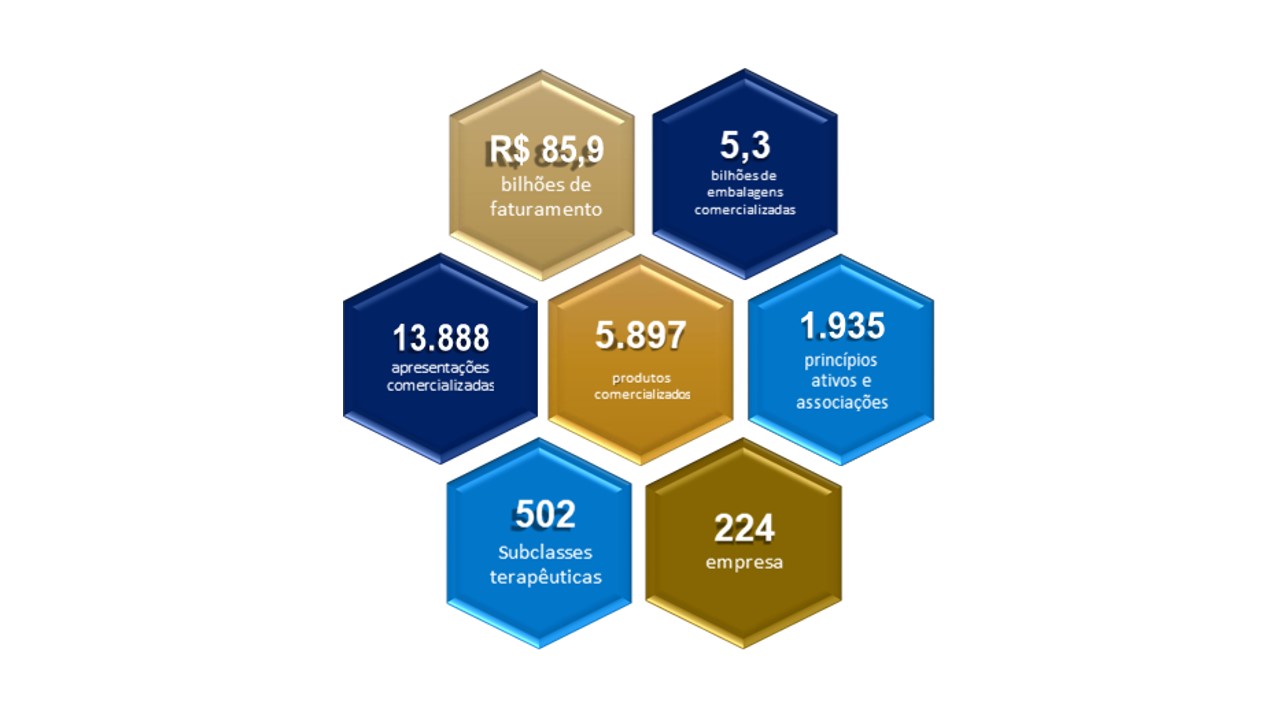
Para saber mais, leia a íntegra da 5ª edição do Anuário Estatístico do Mercado Farmacêutico, com dados de 2019 e séries históricas de 2015 a 2019.
Anvisa divulga novo horário de atendimento presencial
A partir de quarta-feira (14/7), o atendimento presencial na sede da Agência será de segunda a sexta-feira, das 9h às 12h e das 13h às 16h. Entenda!
A Anvisa informa que, a partir desta quarta-feira (14/7), o Serviço de Atendimento ao Cidadão - SIC de forma presencial na sede da Agência, em Brasília (DF), será realizado das 9h às 12h e das 13h às 16h, de segunda a sexta-feira.
Destaca-se ainda que a Central de Atendimento continuará a funcionar das 7h30 às 19h30, pelo telefone 0800 642 9782. Confira aqui os Canais de Atendimento da Agência.
Vacinas contra Covid-19 e eventos adversos: notificações
Nesta matéria, reunimos as principais informações sobre notificação de eventos adversos de vacinas contra Covid-19. Confira
Você foi vacinado contra Covid-19, sentiu algum desconforto e acredita que esse desconforto está relacionado ao imunizante recebido? Acesse o sistema eletrônico VigiMed e notifique a suspeita de evento adverso. O preenchimento é simples, com poucos campos obrigatórios, e você irá subsidiar ações de monitoramento da segurança desses produtos, colaborando com a detecção de sinais em todo o mundo!
A Anvisa vem se preparando desde o início da pandemia para aprimorar a comunicação de eventos adversos pós-vacinais. Em 24/5, a Agência realizou um encontro com fabricantes e detentores de registro das vacinas distribuídas no país a fim de prestar orientação para a melhoria da qualidade das notificações dos eventos adversos no VigiMed. O objetivo é agilizar a análise de causalidade, ou seja, a investigação sobre a relação entre o evento adverso e a vacina administrada.
Neste momento, você que lê esta matéria deve estar se perguntando: se as vacinas são tão seguras, por que a preocupação com os eventos adversos?
Estamos tratando de tecnologias novas, de produtos inovadores, e é dever da autoridade sanitária prezar pelo monitoramento deles para verificar sua segurança e efetividade. Essa ação não surgiu com a pandemia do novo coronavírus. O acompanhamento de produtos para saúde introduzidos no mercado sempre foi feito por uma equipe técnica especializada. É a razão de existir da gerência de Farmacovigilância da Anvisa. Ocorre que, no caso da Covid-19, esse cuidado tem de ser intensificado devido ao uso em larga escala de vacinas de diferentes origens, aplicadas ao mesmo tempo, para imunização de toda a população brasileira.
A gerente de Farmacovigilância da Anvisa, Helaine Carneiro Capucho, chama a atenção para a importância das notificações voluntárias de eventos adversos nesse momento em que a vacinação contra Covid-19 está se intensificando. “A subnotificação pode retardar a identificação de sinais de risco e subestimar o tamanho de um problema em potencial. O monitoramento de quaisquer medicamentos e vacinas novos é de fundamental importância para a promoção da saúde. Por isso pedimos que os cidadãos comuniquem suas suspeitas à Agência por meio do VigiMed”, explica.
É também por meio do VigiMed que devem ser notificados eventuais casos de infecção por coronavírus apesar de o indivíduo ter completado a imunização prevista. Ou seja, se a vacina aplicada em você prevê duas doses e você tomou as duas doses e, ainda assim, foi contaminado pelo coronavírus, registre o caso no respectivo sistema eletrônico.
Plano de Monitoramento
Em 15/1, a Anvisa divulgou o Plano de Monitoramento de Eventos Adversos de Medicamentos e Vacinas Pós-Autorização de Uso Emergencial: Diretrizes e Estratégias de Farmacovigilância para o Enfrentamento da Covid-19. O documento abrange atividades já desenvolvidas pela área de Farmacovigilância da Agência em sua rotina, lições aprendidas com epidemias anteriores (na cooperação entre autoridades reguladoras de vários países do mundo) e estratégias específicas para monitorar os produtos destinados à pandemia de Covid-19.
Para se ter uma ideia da sua amplitude, o Plano de Monitoramento estabelece diretrizes e estratégias para apoiar a tomada de decisão regulatória em farmacovigilância durante a pandemia e se baseia no Sistema de Notificação e Investigação de Produtos em Vigilância Sanitária, nas Boas Práticas de Farmacovigilância, nas recomendações de organismos internacionais e no Programa Nacional de Imunização, o PNI.
A Anvisa, aliás, firmou uma articulação estratégica com o PNI para vigilância epidemiológica e sanitária dos eventos adversos pós-vacinação. Isso inclui, por exemplo, ações para o monitoramento dos vacinados, processos de investigação epidemiológica, avaliação dos casos e classificação de causalidade. As ações com o PNI constituem, portanto, um braço importante para as ações de farmacovigilância das vacinas no setor público.
Clínicas privadas de vacinação
Até o momento, não existe clínica privada autorizada pela Anvisa que possa oferecer vacinas contra Covid-19. Vale ressaltar que as clínicas privadas só poderão oferecer essas vacinas com expressa autorização da Agência. De olho no futuro, caso as vacinas sejam disponibilizadas nessas clínicas, a Anvisa publicou a Nota Técnica (NT) 49/2020.
A NT 49/2020 reúne uma série de requisitos sobre o monitoramento de eventos adversos, além de reforçar a necessidade de notificação. Ou seja, as empresas, quando autorizadas a ofertar vacinas contra Covid-19, deverão seguir rigorosamente o disposto no documento.
A Nota Técnica também orienta as Vigilâncias Sanitárias locais a respeito dos procedimentos necessários ao cumprimento das determinações da legislação sanitária federal. Durante as inspeções realizadas em clínicas privadas de vacinação, a Anvisa reforça a importância de se confirmar se esses serviços de saúde têm cadastro no VigiMed para notificação de eventos adversos pós-vacinais. Portanto, as clínicas privadas que tenham a intenção de comercializar esses produtos já devem pedir o cadastro no respectivo sistema para registro dos possíveis eventos adversos.
Leia também:
Notificação de evento adverso: tudo o que você precisa saber
Como notificar eventos adversos a medicamentos e vacinas?
Evento adverso: o que a Anvisa faz com a sua notificação
Centro de Monitorização de Medicamentos completa 20 anos
Fonte: Anvisa, em 12.07.2021
