A proposta dispõe sobre os procedimentos a serem adotados para distribuição dos processos pendentes de registro de produtos técnicos equivalentes, pré-misturas e produtos formulados de agrotóxicos e afins e visa atender ao Decreto nº 10.833/2021.
Foi publicada, por meio da Portaria SDA n° 737, de 30 de dezembro de 2022, Consulta Pública (CP) referente à proposta de norma conjunta que trata da regularização de produtos agrotóxicos, a ser editada pelo Ministério da Agricultura, Pecuária e Abastecimento (MAPA), Instituto Brasileiro do Meio Ambiente e dos Recursos Naturais Renováveis (Ibama) e Agência Nacional de Vigilância Sanitária (Anvisa).
O processo regulatório encontra-se sob condução do MAPA e seguirá o fluxo administrativo definido no Despacho n° 1, de 2 de janeiro de 2023, da Diretoria Colegiada da Anvisa (https://www.in.gov.br/web/dou/-/despacho-n-1-de-2-de-janeiro-de-2023-455763621), nos termos do Voto n° 335/2022/SEI/DIRE3/ANVISA.
Assim, as sugestões, tecnicamente fundamentadas, deverão ser encaminhadas por meio do Sistema de Monitoramento de Atos Normativos - SISMAN, da Secretaria de Defesa Agropecuária - SDA/MAPA, por meio do link: https://sistemasweb.agricultura.gov.br/sisman/.
A CP estará aberta para contribuições por 60 dias, a contar do dia 2 de janeiro de 2023. Destaca-se que todas as contribuições recebidas serão avaliadas conjuntamente com a participação dos três Órgãos envolvidos no tema.
A proposta normativa visa estabelecer procedimentos específicos para avaliação dos processos pendentes de análise quando da publicação do Decreto n° 10.833, de 7 de outubro de 2021, atendendo ao disposto em seu Artigo 3°. O referido dispositivo estabelece o prazo de quatro anos, iniciado em 08 de outubro de 2021, para que os órgãos anuentes no registro de um agrotóxico possam avaliar os processos pendentes.
A norma tem como objetivo otimizar a avaliação de produtos à base dos mesmos ingredientes ativos, uma vez que produtos de mesmo ativo tendem a apresentar características toxicológicas, ecotoxicológica e de eficiência agronômica semelhantes e, com isso, favorecer uma análise sistematizada dos processos pendentes. No entanto, destaca-se que a otimização da análise não irá prejudicar a análise toxicológica (pela ANVISA) ou de eficácia (pelo MAPA).
Reitera-se que a simplificação na análise dos produtos não compromete o controle exercido pelos órgãos anuentes do registro, por se tratarem de produtos de composição quali-quantitativa idêntica a outros já registrados, avaliados ou submetidos à avaliação, os quais servirão como referência para o registro.
Acesse aqui a Minuta de CP e o Voto 335/2022/SEI/DIRE3/ANVISA.
Audiência Pública promovida pela Anvisa discute atividades referentes a exames de análises clínicas
Objetivo do encontro foi ampliar o diálogo sobre a proposta de Resolução que trata dos requisitos técnico-sanitários para o funcionamento de serviços que executam atividades relacionadas a exames de análises clínicas
Aproposta de regulação da Anvisa que trata dos requisitos técnico-sanitários para o funcionamento de laboratórios clínicos, laboratórios de anatomia patológica e outros serviços que executam atividades relacionadas a exames de análises clínicas (EACs) foi apresentada nesta quarta-feira, 11/01, em audiência pública.
O texto em discussão foi antecipado a toda a sociedade por meio de disponibilização no portal da Agência no dia 20/12/2022 no link.
A proposta da Anvisa traz pontos importantes que podem ser divididos em dois grandes eixos: atualização dos requisitos de gestão da qualidade e controles que devem ser observados pelos serviços que realizam atividades relacionadas a exame de análises cínicas e regulamentação da execução “testes rápidos” por outros estabelecimentos de saúde além daqueles previstos na legislação vigente, com foco no acesso e segurança do usuário.
Na abertura do evento, o Diretor da Anvisa, Alex Machado Campos, ressaltou a importância da interlocução da Agência com todos os atores afetos ao tema e fez referência ao histórico do processo regulatório. Nesse sentido, destacou os diálogos empreendidos desde o pedido de vista ao processo regulatório, ocorrido em julho/2022, a fim de que a minuta de Resolução fosse objeto de amplo debate com a sociedade. Por fim, ressaltou o compromisso da Diretoria em realizar um debate técnico e amadurecido para aprimoramento do texto, reafirmando a robustez do setor de diagnósticos no Brasil.
Durante o evento, a equipe técnica da Anvisa reiterou a importância de participação da sociedade e agradeceu a todas as contribuições recebidas durante a construção do processo regulatório. Também destacou que o eixo central da proposta é o laboratório clínico, o qual atua como indutor da política de qualidade dos exames de análises clínicas. Ademais, ressaltou a evolução do setor de diagnósticos e de serviços, fazendo-se necessária a modernização da RDC nº 302/2005 frente à realidade atual.
Destaca-se que as contribuições escritas dos participantes poderão ser realizadas por meio de formulário próprio, que ficará disponível até às 14h30min do dia 16/1, no link.
O relatório da Audiência Pública, contendo o número de presentes, o registro sintético da reunião e o número de manifestações ocorridas será disponibilizado no sítio eletrônico da Anvisa em até 30 (trinta) dias após o seu encerramento.
Confira a apresentação da Audiência Pública nº 11/2022 e acesse os documentos relacionados a Audiência no link.
Anvisa divulga número de produtos de base biológica aprovados em 2022 para uso na agricultura
Em comparação ao ano de 2021, houve um aumento de 70% de produtos avaliados.
O número de aprovações de produtos de base biológica para o controle de pragas e de doenças na agricultura vem crescendo no país. De acordo com dados da Anvisa, em 2022 foram finalizadas as análises de um total de 157 pedidos deste tipo, representando um aumento de 70% em relação às solicitações concluídas em 2021. O crescimento na quantidade de avaliações para fins de registro de produtos destinados ao controle biológico na agricultura pode ser considerado um marco, segundo a Agência. Confira no gráfico abaixo a evolução do número de aprovações desde 2016.
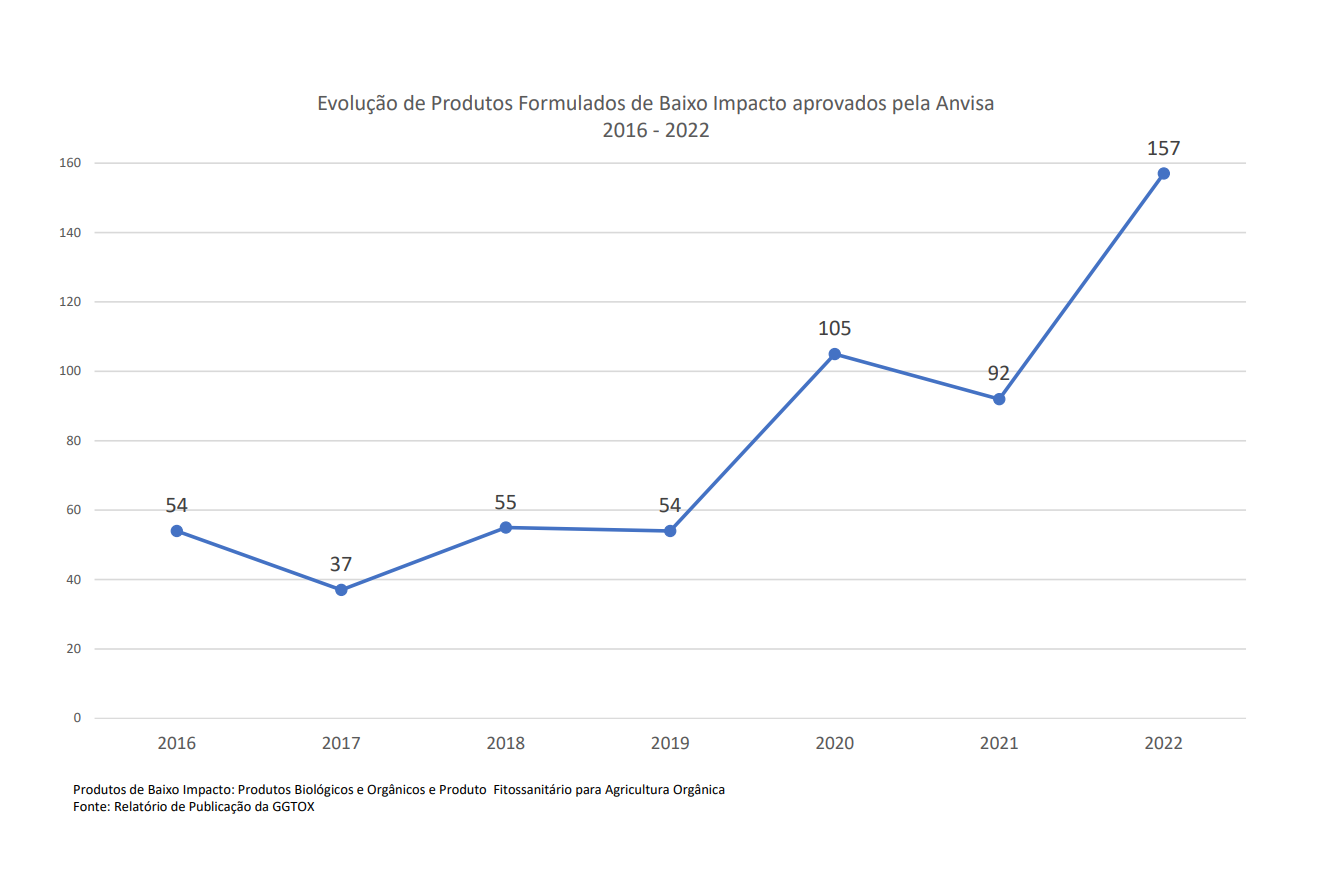
A análise desses produtos é realizada de forma prioritária, sendo que o tempo médio atualmente praticado pela Agência para a conclusão desse tipo de análise é de quatro meses. A série histórica, referente aos pedidos analisados e aprovados pela Anvisa, demonstra uma mudança de comportamento do mercado ao longo do tempo, quanto à adoção dessas práticas no combate de pragas agrícolas.
Entenda
Os produtos de base biológica para o controle de pragas e doenças na agricultura são agrotóxicos desenvolvidos a partir de algum ingrediente ativo que possua origem natural. Esse ativo biológico pode consistir em agentes macrobiológicos (ácaros, insetos e nematoides), microbiológicos (vírus, bactérias e fungos), semioquímicos (feromônios), bioquímicos (hormônios) e fitoquímicos (à base de plantas).
O controle biológico de pragas e doenças na agricultura é uma prática secular. Esses ativos agem com o objetivo de eliminar a praga-alvo, com baixo risco de agressão à saúde humana e ao meio ambiente, permitindo a manutenção do equilíbrio do ecossistema em que são inseridos e o manejo sustentável de pragas e doenças. Consequentemente, o controle biológico de pragas proporciona menor presença de resíduos químicos nos alimentos e no meio ambiente.
Verifica-se uma tendência de crescimento na adoção desse tipo de tecnologia pela agricultura brasileira. Prova disso é que, nos últimos anos, no Brasil, houve um aumento expressivo de registros de produtos com a finalidade de controle biológico de pragas na agricultura. Só em 2019, o mercado nacional desse tipo de produto movimentou R$ 675 milhões, crescimento da ordem de 15% em relação a 2018, e acima da média estimada de crescimento internacional, conforme apontou, em 2021, o Ministério da Agricultura, Pecuária e Abastecimento (Mapa).
É oportuno destacar, ainda, um outro indicador importante: o total de monografias de ingredientes ativos autorizados no Brasil para uso agrícola, o que demonstra o crescimento pelo interesse de produtos de base biológica e demais produtos de baixo impacto na saúde da população. Atualmente, existem 470 monografias de ingredientes ativos publicadas, cerca de 430 aprovadas para uso agrícola, dos quais 130 são de base biológica e compostos inorgânicos, cujos produtos são considerados de baixa toxidade, o que representa 28% do total de ingredientes ativos autorizados no país.
Fonte: Anvisa, em 12.01.2023.
