Orientação é que os serviços de saúde verifiquem as embalagens minuciosamente e, caso identifiquem características de falsificação, não utilizem os produtos.
A Anvisa determinou, por meio da Resolução RE 245, de 27 de janeiro de 2022, a apreensão e a proibição da distribuição, da comercialização e do uso de unidades falsificadas do lote IVL1915/50 do medicamento Inmunoglobulina G Endovenosa.
O fabricante do produto (Laboratório de Hemoderivados da Universidade Nacional de Córdoba), localizado na Argentina, comunicou à Agência a falsificação do frasco-ampola de solução injetável de imunoglobulina de 5g/100 mL, que apresenta as seguintes divergências em relação ao medicamento original:
- o formato e o tamanho do frasco são diferentes;
- não estão presentes no produto falsificado o número do lote e a data de validade gravados no lacre, informações que constam no medicamento original;
- o tipo de letra, a codificação de lote e validade na embalagem secundária apresentam diferenças entre o produto original e o falsificado.
Assim sendo, a Anvisa solicita aos serviços de saúde que, caso recebam unidades de imunoglobulina fabricadas pelo Laboratório de Hemoderivados da Universidade Nacional de Córdoba, antes de utilizá-las, façam uma verificação minuciosa da embalagem e do rótulo do produto.
Caso sejam identificadas unidades com as características de falsificação descritas acima, não utilizem os produtos e comuniquem o fato imediatamente à Agência, preferencialmente por meio do sistema Notivisa.
Confira abaixo as diferenças entre o produto original e o falsificado.
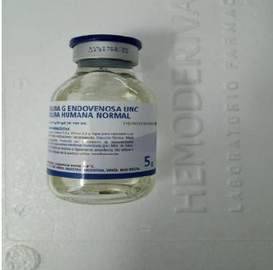
Produto original
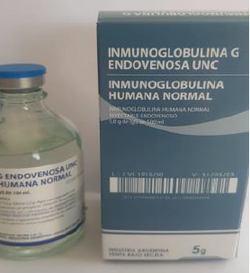
Produto falsificado
Anvisa atualiza Agenda Regulatória para o ano de 2022
Revisão anual do documento resultou em 30 alterações/atualizações, 27 inclusões e 13 exclusões de projetos regulatórios. Entenda!
A Diretoria Colegiada da Anvisa acaba de aprovar a atualização anual da Agenda Regulatória 2021-2023, originalmente publicada em maio de 2021. A medida foi deliberada nesta quarta-feira (9/2), durante a 2ª Reunião Ordinária Pública da Agência.
Como previsto no Documento Orientador da Agenda Regulatória - AR 2021-2023, o conjunto de projetos regulatórios da Agenda pode ser revisado anualmente, com a possibilidade de alterações, exclusões e inclusões de projetos. O objetivo da atualização anual é manter o documento alinhado às prioridades regulatórias do período, para garantir a previsibilidade e a atualidade do planejamento regulatório da Agência.
Nesta primeira revisão anual, houve a seguinte mudança em relação aos projetos da Agenda 2021-2023: 30 alterações/atualizações, 27 inclusões e 13 exclusões de projetos. Destaca-se que ocorreu um aumento considerável de projetos regulatórios relacionados a medicamentos, área de atuação da Anvisa que concentrou quase 50% (13) dos novos projetos incluídos na Agenda. Essa atualização anual será publicada no Diário Oficial da União (D.O.U.).
A partir das atualizações consolidadas, a nova lista atualizada de projetos regulatórios da Agenda da Anvisa para o período 2021-2023 passa a ser composta por 158 projetos regulatórios, distribuídos por 16 macrotemas de atuação da Agência. Consulte a listagem em planilha, com o detalhamento dos projetos e as respectivas justificativas para as alterações e exclusões realizadas.
Confira ainda a página específica da Agenda Regulatória 2021-2023 no portal.
Processo de atualização da Agenda
As atividades para a primeira atualização da Agenda foram iniciadas em dezembro de 2021 e se estenderam até fevereiro de 2022, conforme descrito no Relatório de Atualização Anual da Agenda 2021-2023. Para a atualização dos projetos, foram aplicados os mesmos critérios previstos na construção da Agenda Regulatória, que compreendem o alinhamento dos projetos aos objetivos estratégicos da Anvisa e a previsão de atividades no ano atual da Agenda. Isso significa que, para a inclusão ou manutenção de projetos, é necessária a realização de uma ou mais etapas regulatórias ao longo do ano de 2022.
Além desses dois critérios, foram consideradas como fontes para a atualização dos projetos as contribuições recebidas na consulta externa para a construção da Agenda, realizada entre 23 de novembro de 2020 e 22 de janeiro de 2021, bem como informações sobre o acompanhamento dos instrumentos e dos processos regulatórios em andamento na Anvisa.
A partir desses dados, as áreas registraram as atualizações de projetos e as Diretorias Supervisoras, no papel de integrantes da Comissão Executiva de Acompanhamento da Agenda, validaram os indicativos para a atualização anual de 2022 da Agenda.
Fonte: Anvisa, em 09.02.2022.
