A Agência acompanha o cenário epidemiológico da prevalência da nova variante.
A Anvisa solicitou em 1/12/2021 às desenvolvedoras de vacinas autorizadas no Brasil, informações sobre os estudos em andamento.
A solicitação foi encaminhada aos laboratórios Pfizer, Butantan, Fiocruz e Janssen. A Anvisa exige, para as vacinas autorizadas, que os desenvolvedores monitorem e avaliem o impacto das variantes na eficácia e na efetividade dos imunizantes. É preciso observar, porém, que esses estudos demandam tempo, uma vez que é preciso obter informações genéticas e amostras de pacientes para então realizar os testes e a análise.
Foi dado prazo de uma semana para as empresas se manifestarem e em 8/12/2021, ao final desse prazo:
- a Pfizer e Fiocruz encaminharam as estratégias que estão sendo tomadas, em resposta ao ofício.
- o Instituto Butantan solicitou prazo até segunda-feira, dia 13/12/2021, visto que aguardam algumas discussões e definições internas para que possam responder ao ofício; e
- a Janssen ainda não se manifestou.
A Gerência Geral de Medicamentos e Produtos Biológicos avaliará os dados encaminhados e continuará o monitoramento dos estudos relativos à variante Ômicron. A Agência também acompanha o cenário epidemiológico da prevalência dessa variante e a ausência das informações solicitadas pode prejudicar a manutenção da atual autorização da Anvisa.
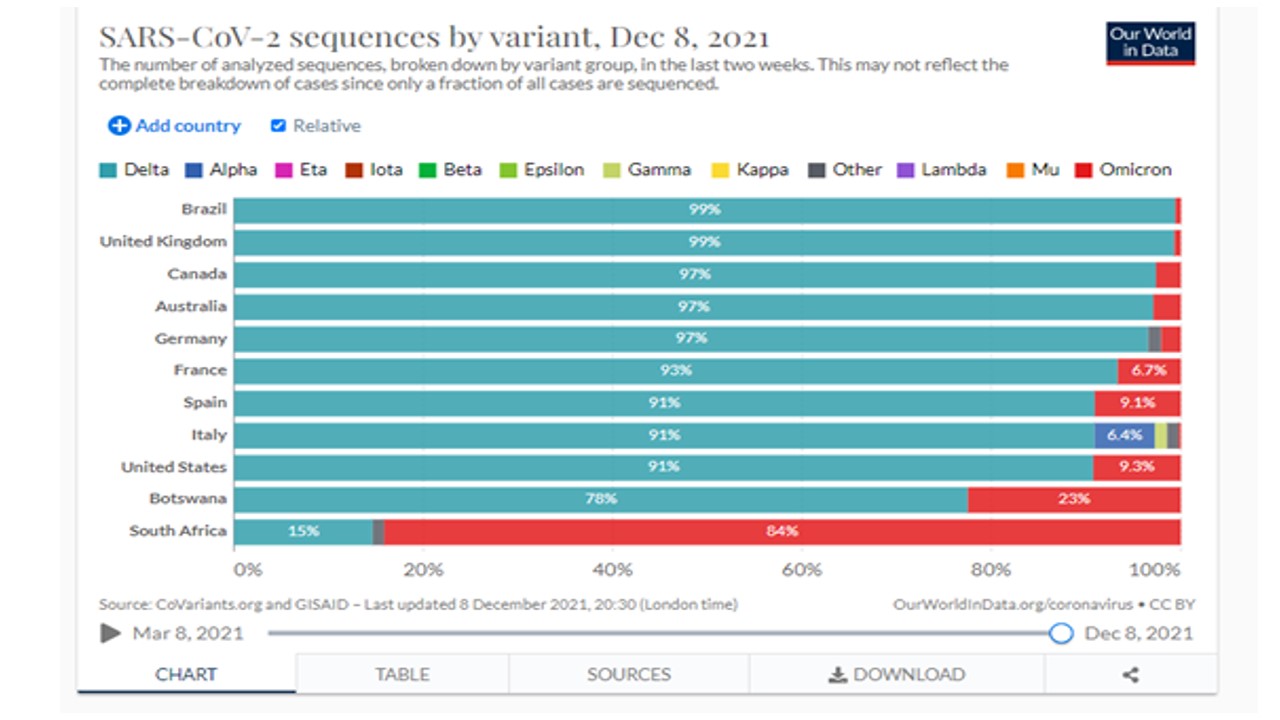
Importante esclarecer que a avaliação experimental completa da Ômicron pode levar semanas ou até meses. Entretanto, os desenvolvedores de vacinas devem manter a vigilância permanentes dos seus imunobiológicos frente ao aparecimento da variante de preocupação
A variante Omicron contém muitas mutações da proteína spike, bem como mutações em outras partes do genoma viral, com indicações iniciais sugerindo que essa variante pode ser mais transmissível.
Reforçamos, baseados em tudo o que sabemos, que as nossas vacinas continuam sendo nossa melhor linha de defesa e todos que ainda não receberam sua primeira ou segunda dose da vacina, ou aqueles que são elegíveis para seu reforço, são encorajados a se apresentar para ajudar a proteger a si próprio e ao coletivo.
O programa de vacinação, a ampla testagem, o rastreamento genômico e a adoção das medidas não farmacológicas (uso de máscaras, distanciamento social, higienização das mãos) continuam sendo essenciais para o enfrentamento da pandemia, independente da variante Ômicron.
A Anvisa manterá o trabalho ativo com os reguladores internacionais e desenvolvedores dos imunizantes para possibilitar uma atuação rápida diante de potenciais impactos da nova variante Ômicron nas vacinas contra Covid-19 usadas no Brasil.
Anvisa informa mudança no calendário de reuniões da Dicol
A próxima reunião ocorrerá no dia 17 de dezembro (sexta-feira).
A Secretaria Geral da Diretoria Colegiada (SGCol) da Anvisa informa a mudança no calendário de reuniões da Diretoria Colegiada (Dicol). A próxima Reunião Ordinária Pública (ROP) está programada para o dia 17 de dezembro, a partir de 9h30. A última reunião do ano será realizada por meio de videoconferência, conforme o Decreto nº 10.416, de 7 de julho de 2020.
Clique aqui e fique por dentro do calendário de reuniões da Diretoria Colegiada em 2021.
Veja a pauta republicada.
Anvisa aprova norma que altera critérios para embalagens plásticas e celulósicas
Regulamentos foram harmonizados no Mercosul e passaram por amplo debate com a sociedade.
A Diretoria Colegiada (Dicol) da Anvisa aprovou, nesta quarta-feira (8/12), a resolução que altera as regras para embalagens e outros materiais em contato com alimentos. A medida foi tratada durante a 19ª Reunião Extraordinária Pública da Dicol.
Ao total, foram atualizadas três normas: a Resolução - RES 105/1999 e as Resoluções da Diretoria Colegiada (RDCs) 88/2016 e 56/2012, as quais internalizam, respectivamente, as Resoluções GMC 56/1992, 40/2015 e 02/2012, no âmbito do Mercosul.
Nesse sentido, é importante esclarecer que a primeira norma, a Resolução 105/1999, trata das disposições gerais para embalagens e equipamentos plásticos em contato com alimentos. Ela foi revista com o objetivo de atualizar os limites de migração total e as restrições relativas a corantes, de forma a compatibilizar a norma com os regulamentos mais recentes harmonizados no âmbito do Mercosul e com as referências internacionais.
A RDC 56/2021 dispõe sobre a lista positiva de monômeros, outras substâncias iniciadoras e polímeros autorizados para elaboração de embalagens e equipamentos plásticos em alimentos. Os objetivos da atualização deste regulamento foram:
proteger a saúde da população, por meio da redução do limite de migração específica de bisfenol A, uma substância investigada como potencial desreguladora do sistema endócrino, cujos efeitos na fertilidade, reprodução e sistema endócrino têm sido objeto de debate científico; e
contribuir para a inovação tecnológica na elaboração de embalagens plásticas, por meio da atualização das listas positivas, da incorporação de novas substâncias aprovados pela Anvisa e de substâncias incluídas nas atualizações do regulamento europeu utilizado como referência, além da compatibilização com regulamento do Mercosul atualizado recentemente (Resolução GMC 39/2019).
Já a RDC 88/2016 trata dos materiais, embalagens e equipamentos celulósicos destinados a entrar em contato com alimentos. Este regulamento foi revisado para atualizar a lista positiva de componentes para esses produtos (materiais, embalagens e equipamentos celulósicos), por meio da incorporação de novas substâncias aprovadas pela Agência em decorrência das petições protocoladas pelo setor produtivo.
Por fim, destaca-se que a publicação dessa norma foi resultado de um processo regulatório amplo e transparente, iniciado em 2020, com a publicação, em 21 de julho daquele ano, do Termo de Abertura de Processos – TAP 83. Em seguida, a proposta normativa foi submetida a consulta pública (CP 897/2020), ocasião em que recebeu cerca de 25 contribuições de diversos grupos da sociedade.
A Gerência-Geral de Alimentos (GGALI) da Anvisa também realizou, em fevereiro de 2021, um diálogo setorial no qual todas as questões apresentadas na consulta pública foram esclarecidas e discutidas com os interessados. Após esse debate, o prazo de adequação à proposta foi ampliado para 12 meses.
Saiba mais
A regulamentação de materiais em contato com alimentos é uma atribuição da Anvisa prevista no art. 8º, §1º, inciso II, da Lei 9.782/1999 e na RDC 91/2001, que estabelece que os componentes utilizados nos materiais destinados ao contato com alimentos devem estar incluídos em listas positivas de substâncias consideradas seguras.
A regulação do tema está sujeita à harmonização junto aos demais países do Mercosul e depende de consenso entre os membros do bloco.
Clique aqui e veja mais informações sobre a regulação de embalagens pela Anvisa.
Anvisa promove oficina para servidores sobre cadeia de valor
Evento se soma às atividades que vêm sendo realizadas para modernização da gestão estratégica da Agência.
Cento e cinco servidores participaram da oficina sobre cadeia de valor e construção do modelo de negócio da Anvisa, realizada em parceria com o Ministério da Economia. O evento reflete o compromisso da Agência com as ações do Programa de Gestão Estratégica e Transformação do Estado (TransformaGov).
A partir de agora, a ideia é avançar na representação e na transparência das atividades executadas e suas relações com os valores gerados pela Anvisa. Além disso, espera-se proporcionar melhorias no acompanhamento dos resultados alcançados e na comunicação com a sociedade sobre as principais entregas, de modo a fortalecer a visão estratégica e a capacidade de gestão da Agência.
O projeto deverá ser concluído no primeiro trimestre de 2022, com a publicação da nova cadeia de valor. Até lá, uma série de etapas estão previstas, como a reformulação da nova cadeia de valor e a validação da respectiva proposta com as unidades organizacionais e a diretoria da Anvisa.
Entenda
A Anvisa aderiu ao TransformaGov em 19 de novembro de 2020. O programa, instituído pelo Decreto 10.382/2020, tem como objetivo avaliar e modernizar a gestão estratégica dos órgãos integrantes da administração pública federal direta, autárquica e fundacional. O programa reúne um conjunto de soluções de curto e médio prazo já desenvolvidas pelo Ministério da Economia para apoiar os órgãos no desenvolvimento de novas soluções de aprimoramento da gestão.
Anvisa informa mudança nas petições de produtos de tabaco
A partir da próxima quarta-feira (15/12), a Agência implementará um novo fluxo para petições de produtos fumígenos. Entenda!
A Anvisa irá disponibilizar, a partir da próxima quarta-feira (15/12), um novo fluxo para petições de Transferência de Titularidade, Desistência de petição/processo a pedido, Aditamento, Cancelamento de Registro de Produto Fumígeno a Pedido e Reconstituição de Documentação.
As referidas petições deverão ser protocolizadas exclusivamente por meio de peticionamento eletrônico (Sistema Solicita), utilizando os códigos de assunto listados abaixo:
|
6067
|
Transferência de Titularidade
|
|
6055
|
Desistência de petição/processo a pedido
|
|
6031
|
Aditamento
|
|
6010
|
Cancelamento de Registro de Produto Fumígeno a Pedido
|
|
6036
|
Reconstituição de Documentação
|
Destaca-se que a medida é resultado do aprimoramento realizado pela Agência. O objetivo é padronizar os procedimentos e dar mais agilidade a essas demandas. Com o envio eletrônico dessas petições, o expediente será imediatamente protocolizado e vinculado ao processo, acelerando sua análise.
No caso das petições de aditamento (assunto 6031), ressalta-se que estas não serão consideradas quando a análise da petição a que se vinculam já estiver finalizada (análise concluída).
É importante enfatizar ainda que esses assuntos podem ser vinculados a petições primárias ou secundárias e que a correta vinculação é feita pela empresa durante o peticionamento. Dessa forma, vincular o aditamento ao expediente correto é essencial para a localização da complementação enviada.
Conforme a Resolução da Diretoria Colegiada (RDC) 204/2005, os aditamentos devem ser utilizados para toda e qualquer complementação ao processo, não exigida formalmente, que se limita ao aprimoramento do conhecimento do objeto do processo, não resultando em manifestação diversa da peticionada. Sendo assim, um aditamento nunca deverá ser utilizado como petição de pós-registro.
Por fim, faz-se necessário esclarecer que não serão mais disponibilizados os seguintes códigos: 6056 - Aditamento para cumprimento do art. 34 da Resolução RDC 226/18 e 6058 - Aditamento para Cumprimento de Exigência, exclusivo para atendimento ao § 3º do art. 15 da RDC 226/18.
Fonte: Anvisa, em 08.12.2021.
