Insumos farmacêuticos da Formus Magistral são proibidos
Empresa importou anabolizante e hormônio não permitidos. Saiba mais.
Uma ação de fiscalização da Anvisa, publicada nesta quarta-feira (7/1), proibiu dois insumos farmacêuticos da Formus Magistral Comércio de Insumos Farmacêuticos Ltda. A empresa importou, de maneira irregular, o anabolizante estanozolol e o hormônio prasterona.
Estão proibidos, portanto, o armazenamento, a comercialização, a distribuição, a importação, a manipulação e o uso desses insumos.
Farma Vida
Outra empresa atingida pela ação fiscal foi a Drogaria Farma Vida de Janaúba Ltda. Com isso, a comercialização e a divulgação dos seus produtos estão suspensas.
O motivo da suspensão é o fato de a empresa estar anunciando e comercializando medicamentos manipulados, através de seu site de vendas on-line, sem prescrição médica. Esta prática não é permitida, conforme estabelece o item 5.14 do Anexo – Regulamento Técnico, que institui as Boas Práticas de Manipulação em Farmácias (BPMF), da Resolução da Diretoria Colegiada (RDC) 67/2007.
Leia a íntegra da medida publicada no Diário Oficial da União.
Anvisa determina recolhimento de medicamentos com irregularidades, e apreende e proíbe medicamentos falsificados
Saiba quais os medicamentos atingidos pela ação de fiscalização da Agência.
A Anvisa determinou, nesta quarta-feira (7/1), o recolhimento do lote OA3169 do medicamento Pantoprazol Sódico Sesqui-Hidratado – 40mg, indicado para o tratamento de problemas gastrointestinais. Apenas o lote citado foi atingido pela ação, que ainda suspendeu a sua comercialização, distribuição e uso.
A medida foi adotada após a empresa MedQuímica Indústria Farmacêutica Ltda. comunicar o recolhimento voluntário do lote, ou seja, a ação partiu da própria fabricante, que identificou a irregularidade em seu produto. A caixa do Pantoprazol 40mg foi trocada pela embalagem de outro medicamento, a Hidroclorotiazida 25mg, indicada para tratar pressão alta.
Antialérgico
O lote 569889 do antialérgico Alektos 20mg, da empresa Cosmed Indústria de Cosméticos e Medicamentos S.A., também deve ser recolhido e teve a sua comercialização, distribuição e uso suspensos.
Isso porque, depois de identificar que a embalagem do Alektos 20mg havia sido trocada pela do medicamento Nesina, a empresa comunicou o recolhimento voluntário do lote em questão.
Lotes falsos
Lotes falsificados dos medicamentos Imbruvica, Mounjaro e Voranigo também foram alvo de ação fiscal da Agência, que determinou a sua apreensão e proibição.
Imbruvica
Os lotes NIS7G01, NJS7J00 e PJS0B00 do medicamento Imbruvica, indicado no tratamento de diversos tipos de câncer no sangue, devem ser apreendidos e estão proibidos de ser comercializados, distribuídos e usados.
A medida foi tomada porque a verdadeira fabricante do medicamento, a Janssen-Cilag Farmacêutica Ltda., informou que não produziu os lotes e que o registro do Imbruvica em formato de cápsulas foi cancelado.
Mounjaro
Conforme comunicado da empresa Eli Lilly do Brasil Ltda., que possui o registro do Mounjaro, o lote D838878 do medicamento não foi fabricado por ela.
Por isso, esse lote deve ser apreendido e não pode ser comercializado, distribuído e usado.
Voranigo
O lote FM13L62 do medicamento Voranigo, para tratar tumores cerebrais, também teve a sua apreensão e proibição determinadas pela Anvisa. Assim, o referido lote não pode mais ser armazenado, comercializado, distribuído, fabricado, importado, divulgado e usado.
Isso porque a empresa Laboratórios Servier do Brasil, que produz o medicamento, desconhece a origem do lote.
Confira a Resolução no Diário Oficial da União.
90 dias da Duimp: balanço inicial aponta avanços e desafios no novo processo de importação
Após três meses da implementação da Declaração Única de Importação, a Anvisa apresenta um balanço com avanços importantes e desafios para ampliar a adesão dos importadores ao novo modelo.
A Declaração Única de Importação (Duimp) completou três meses de implementação no Portal Único de Comércio Exterior (Siscomex). Nesse período, a Anvisa analisou cerca de 320 Duimps nos diferentes canais de parametrização previstos na Resolução da Diretoria Colegiada (RDC) 228/2018. Apesar do progresso, o número ainda é considerado baixo, indicando a necessidade de maior adesão por parte dos importadores.
Importadores têm papel essencial na consolidação do modelo
A participação ativa dos importadores é fundamental para validar cenários e funcionalidades do sistema. Somente com a maior utilização da Duimp será possível identificar ajustes e aprimorar a plataforma.
Funcionalidades testadas no período
Durante os 90 dias, foram avaliados módulos estratégicos do Portal Único, como:
- Gestão de riscos.
- Integração do pagamento da taxa ao Pagamento Centralizado de Comércio Exterior (PCCE).
- Emissão do Relatório de Inspeção Física (RIF).
- Canal único de parametrização entre órgãos anuentes.
Ações conjuntas para melhorias
Como todo sistema novo, ajustes iniciais são necessários para garantir o alinhamento entre funcionalidades e práticas operacionais. A Anvisa atua em conjunto com a Secretaria de Comércio Exterior (Secex) e a Receita Federal para avaliar pontos críticos e implementar melhorias. Erros impeditivos ou procedimentais são reportados por entidades representativas e tratados nas reuniões do Comitê Nacional de Facilitação do Comércio (Confac).
O novo modelo busca oferecer maior agilidade, rastreabilidade e transparência aos processos de importação, assegurando que os produtos cheguem à população com rapidez e segurança sanitária.
A Anvisa convida todos os importadores habilitados, conforme cronograma disponível no Portal Único, a utilizarem a Duimp e contribuírem para a consolidação do Novo Processo de Importação.
Molho de tomate e suplementos alimentares são alvos de ações fiscais
Sistema de comunicação da União Europeia emitiu alerta de que um lote do molho de tomate continha pedaços de vidro. Confira outros alimentos que também sofreram ação fiscal.
A Anvisa determinou, nesta quarta-feira (7/1), o recolhimento do lote LM283 do molho de tomate Passata de Pomodoro Di Puglia, da marca Mastromauro Granoro. Com isso, o lote do produto teve a sua comercialização, distribuição, importação, divulgação e consumo suspensos.
O motivo da suspensão foi o alerta da rede RASFF (Rapid Alert System for Food and Feed – Sistema de Alerta Rápido para Alimentos e Rações) de que o lote do molho de tomate importado para o Brasil continha pedaços de vidro. A rede RASFF é uma ferramenta da União Europeia para a troca rápida de informações sobre riscos graves em alimentos e rações animais.
Suplemento Neovite Visão
Outro produto que deve ser recolhido é o Neovite Visão, suplemento alimentar voltado para a saúde ocular, da empresa BL Indústria Ótica Ltda. (Bausch Lomb).
A ação fiscal atinge apenas os lotes 25G073, S25C004, S25C003, S25C002 e S25G072. Eles estão proibidos de ser comercializados, distribuídos, fabricados, importados, divulgados e consumidos.
Os referidos lotes foram fabricados com Capsicum annuum L. (fruto da páprica), ingrediente não autorizado em suplementos alimentares como fonte de zeaxantina. Além disso, a quantidade de Caramelo IV (caramelo processo sulfito-amônia) nos produtos está acima do limite permitido.
A empresa comunicou o recolhimento voluntário dos lotes. Isso ocorre quando a própria fabricante identifica irregularidades em seus produtos.
Ervas Brasil
Os suplementos de Vitamina C Sucupira com Unha de Gato Ervas Brasil e o Suplemento Alimentar Colesterol Ervas Brasil, da empresa Ervas Brasil Indústria Ltda., também foram alvo de ação de fiscalização sanitária e devem ser apreendidos. Os produtos não podem mais ser comercializados, distribuídos, fabricados, divulgados e consumidos.
A empresa não tem Licença Sanitária e nem Alvará de Funcionamento, e utilizou ingredientes não autorizados em alimentos. Além disso, faz divulgação irregular dos produtos, com falsas indicações terapêuticas, associando o seu uso a benefícios funcionais e de saúde, sem comprovação científica.
Leia as Resoluções no Diário Oficial da União:
- https://www.in.gov.br/en/web/dou/-/resolucao-re-n-33-de-6-de-janeiro-de-2026-679839777
- https://www.in.gov.br/en/web/dou/-/resolucao-re-n-30-de-6-de-janeiro-de-2026-679777819
- https://www.in.gov.br/en/web/dou/-/resolucao-re-n-29-de-6-de-janeiro-de-2026-679838997
Proibida venda de fórmula infantil com risco de contaminação por toxina
Medida é preventiva e fabricante já iniciou o recolhimento voluntário.
Uma medida da Anvisa (Resolução 32/2026), publicada nesta quarta-feira (7/1), determinou a proibição da comercialização, da distribuição e do uso de alguns lotes de fórmulas infantis das marcas Nestogeno, Nan Supreme Pro, Nanlac Supreme Pro, Nanlac Comfor, Nan Sensitive e Alfamino, da empresa Nestlé Brasil Ltda., CNPJ: 60.409.075/0001-52.
A motivação é o risco de contaminação por cereulide, uma toxina produzida pela bactéria Bacillus cereus. O consumo de alimento contaminado por essa toxina pode causar vômito persistente, diarreia ou letargia, que é a sonolência excessiva, lentidão de movimentos e raciocínio, e incapacidade de reagir e expressar emoções.
Recall global
A medida tem caráter preventivo. A fabricante iniciou o recolhimento voluntário no Brasil, assim como no resto do mundo, após a detecção da toxina em produtos provenientes de uma fábrica localizada na Holanda. Foi identificado que a toxina estava presente em um ingrediente proveniente de um fornecedor global de óleos terceirizados. Dessa forma, a empresa indicou a necessidade de um recolhimento global.
No Brasil, os produtos e lotes a serem recolhidos são:
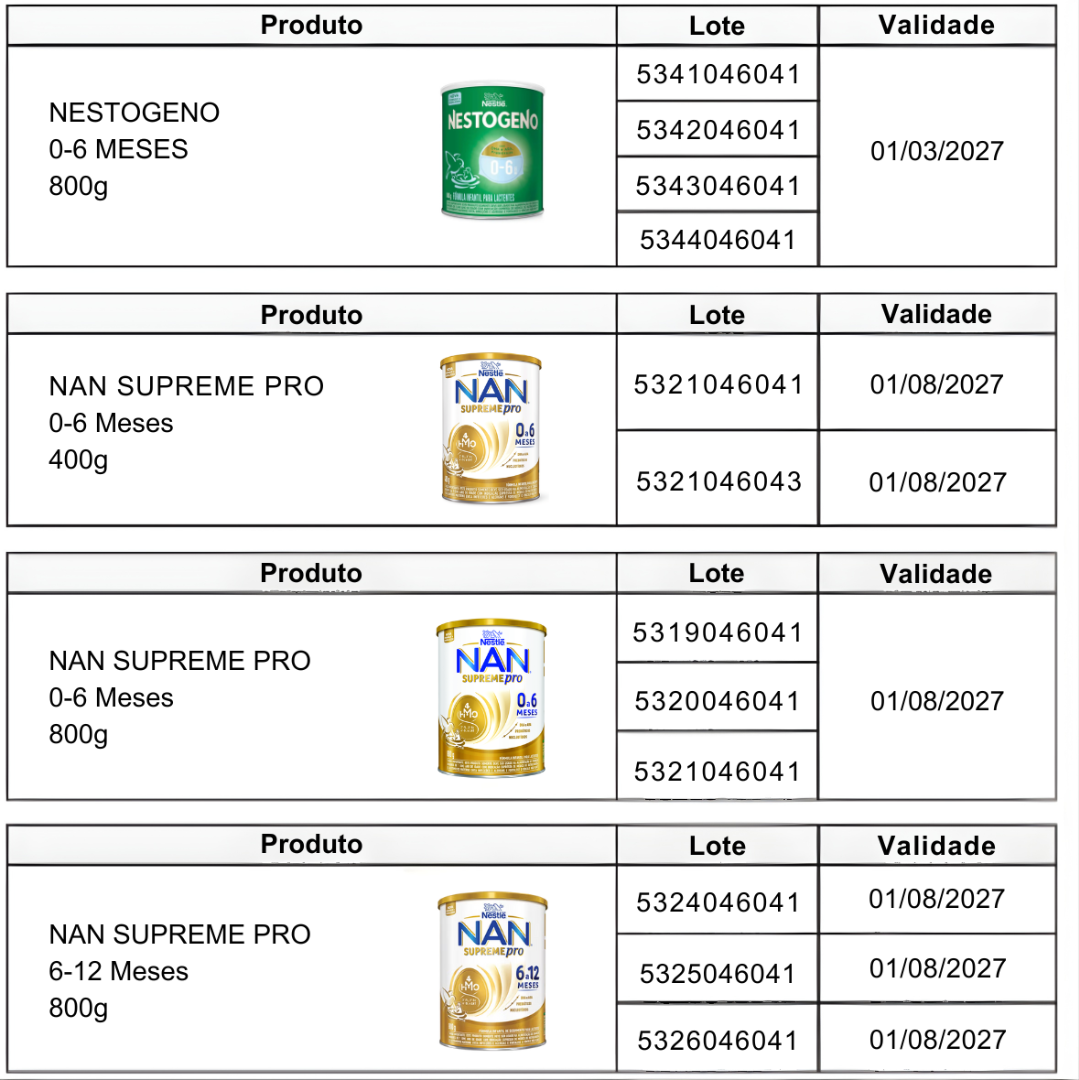
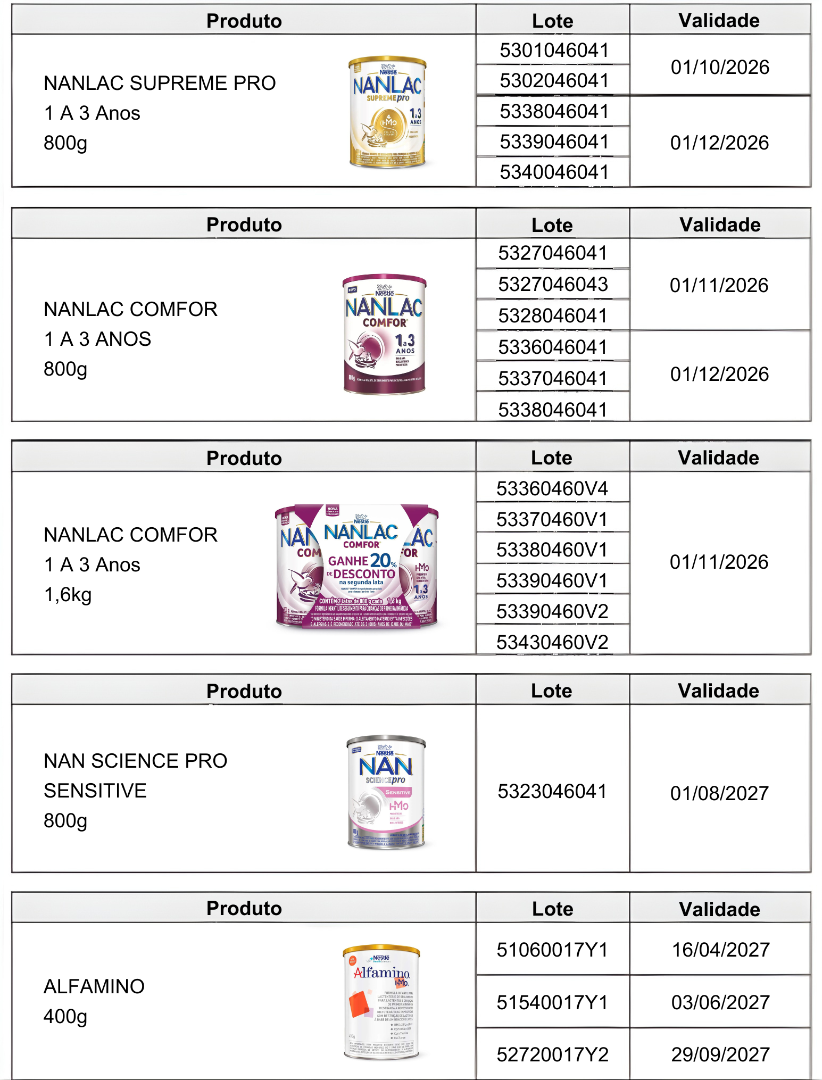
Tabela 2 – Produtos a seres recolhidos
Acesse a íntegra da Resolução 32/2026.
Orientações a pais e responsáveis
Se você utiliza produtos das marcas Nestogeno, Nan Supreme, Nanlac Supreme, Nanlac Comfor, Nan Sensitive e Alfamino, verifique o número do lote impresso no rótulo das fórmulas infantis. Se o produto pertencer a um dos lotes recolhidos, não deve ser utilizado ou oferecido para consumo. Os demais lotes desses produtos não foram afetados.
Para receber orientações sobre como proceder em relação a eventuais trocas e devoluções do produto, entre em contato direto com a Nestlé Brasil Ltda., por meio do Serviço de Atendimento ao Consumidor (SAC), indicado na embalagem.
Se a criança apresentar sintomas compatíveis com os citados acima após o consumo de produto dos lotes indicados, leve-a para atendimento médico. Ao procurar atendimento, é importante informar o alimento que foi consumido, se possível com uma amostra da embalagem, caso tenha disponível.
Saiba mais sobre o uso seguro de fórmulas infantis.
Fonte: Anvisa, em 07.01.2026.
