Anvisa atualiza a Lista de Medicamentos Notificados de Baixo Risco sujeitos à Notificação (LMN)
Instrução normativa foi publicada no Diário Oficial
Foi publicada no último dia 26 de março, por meio da Instrução Normativa (IN) 430/2026, a atualização da IN 106/2026, que estabelece a Lista de Medicamentos de Baixo Risco sujeitos à notificação (LMN).
Esses medicamentos são aqueles para os quais existe baixo risco de que seu uso possa causar consequências ou agravos à saúde quando observadas todas as características de uso e de qualidade previamente estabelecidas.
Todos os medicamentos de baixo risco são de venda isenta de prescrição e a liberação da sua fabricação e comércio não dependem da avaliação prévia da Agência. Para este grupo de medicamentos, basta que as empresas procedam com uma notificação eletrônica à Anvisa antes de iniciar a produção e inserção dos medicamentos no mercado, conforme estabelece a Resolução da Diretoria Colegiada (RDC) 576/2021.
Essa atualização considerou as solicitações de inclusão e alteração protocoladas pelo setor regulado até julho de 2025, além de indicações e revisões técnicas realizadas internamente pela Anvisa, com vistas a assegurar a atualização contínua da LMN e a adequada aplicação do modelo regulatório simplificado de notificação.
Como resultado dessa avaliação, foram incluídos os seguintes medicamentos na LMN:
- paracetamol 500 mg (pó e granulado para solução);
- paracetamol 80 mg e 120 mg (supositório);
- paracetamol 500 mg e 750 mg (cápsula mole);
- cloreto de sódio 20 mg/mL (solução nasal);
- simeticona 250 mg (cápsula dura);
- subsalicilato de bismuto 35 mg/mL (suspensão).
Ainda, foram feitos ajustes na LMN, compreendendo:
- inclusão de advertência quanto ao tempo de uso para todas as apresentações de paracetamol 500 mg e 750 mg, bem como para a concentração de 200 mg/mL;
- adequação à Denominação Comum Brasileira (DCB) de “iodopolividona” para “iodopovidona” em todas as formas farmacêuticas do medicamento;
adequação da posologia pediátrica prevista para o paracetamol 200 mg/mL (solução).
No caso específico da posologia pediátrica do paracetamol 200 mg/mL, a alteração proposta tem por objetivo aprimorar a clareza da orientação de uso constante na LMN, harmonizando a recomendação de dose com a indicação expressa de consulta médica para crianças abaixo de 11 kg ou 2 anos de idade.
O prazo para migração dos medicamentos atualmente registrados para o regime da notificação é de dois anos a partir da vigência da norma, ou seja, até 25 de março de 2028.
Durante o processo de avaliação das solicitações encaminhadas pelo setor regulado, alguns dos pedidos de inclusão na LMN não foram acolhidos pela Anvisa em razão da insuficiência da documentação apresentada, que não permitiu demonstrar de forma adequada o atendimento aos critérios técnicos necessários para enquadramento como medicamentos de baixo risco passíveis de regularização por meio do procedimento simplificado de notificação. Neste sentido, com o objetivo de dar transparência ao processo de avaliação das solicitações, a Agência disponibilizou um documento com um resumo referente às Solicitações de inclusões e alterações na LMN não acatadas pela Anvisa. A publicação traz de forma simplificada as razões técnicas de cada decisão, considerando as solicitações recebidas.
Saiba mais:
O que é e como é o processo de notificação de medicamentos?
A notificação tem por objetivo racionalizar a regularização de medicamentos de baixo risco, que não sofrem análise prévia à sua comercialização, otimizando assim o processo regulatório e o acesso a medicamentos de qualidade.
Nesse processo, as empresas não precisam realizar o protocolo de solicitação de registro sanitário para o medicamento e aguardar a manifestação da Anvisa. Realizando a notificação individual dos medicamentos de baixo risco por meio do sistema eletrônico da Anvisa, as empresas ficam autorizadas a fabricar e comercializar os medicamentos, garantindo mais agilidade e racionalidade na liberação de medicamentos para o mercado.
Os medicamentos notificados devem atender a todos os requisitos de qualidade e serem produzidos conforme as boas práticas de fabricação. As empresas interessadas devem realizar uma notificação para cada medicamento da LMN. A relação de medicamentos notificados pode ser consultada por meio do Portal da Agência, marcando-se a opção de tipo de regularização como medicamento notificado.
Anvisa proíbe autoinjetor de adrenalina sem registro no Brasil
Medicamento não pode ser divulgado nem comercializado no país
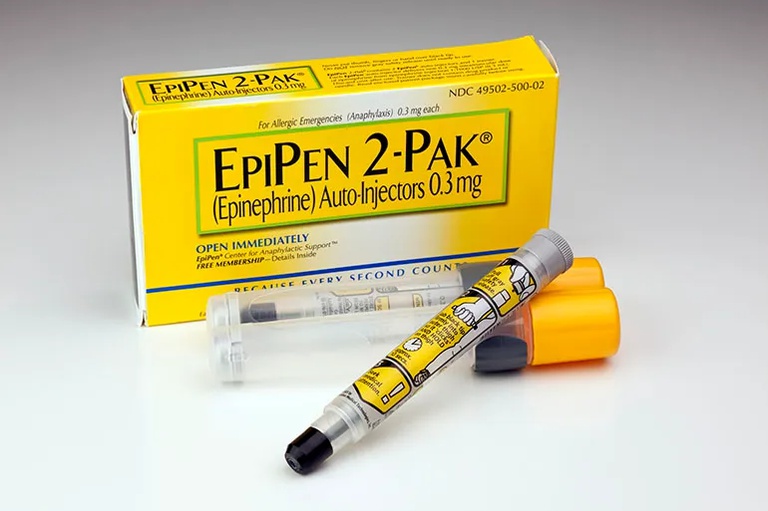
Foto: Divulgação
A Agência Nacional de Vigilância Sanitária (Anvisa) determinou, nesta quinta-feira (2/4), a apreensão do autoinjetor de adrenalina Epipen, importado pela Farmácia Pague Menos. A medida abrange a proibição do armazenamento, da comercialização, distribuição, propaganda e do transporte.
A ação foi motivada por anúncio de venda do medicamento de origem estrangeira sem registro na Anvisa, pela Farmácia Pague Menos.
Medicamentos clandestinos não têm garantia de composição, origem, eficácia e segurança.
Extrato de valeriana
O medicamento fitoterápico Extrato de Valeriana – Foglie Di Tè, fabricado pela empresa Aldeia Produtos Naturais, também foi atingido pela ação de fiscalização. A Agência determinou a apreensão do produto, que não tem licença sanitária. Armazenamento, comercialização, distribuição, fabricação, propaganda, transporte e uso foram proibidos.
Também sem registro na Anvisa, os medicamentos Lucielo 50 Eltrombopag Olamina 50mg Comprimidos e Luciale 150mg Cloridrato de Alectinibe Cápsulas, importados e distribuídos pela Oncomed Distribuidora de Medicamentos e Importação Ltda, também devem ser apreendidos.
Leia a Resolução (RE) 1.280/2026 no Diário Oficial da União
Anvisa determina apreensão de chá produzido em galpão clandestino
Chá misto Protocolo RMGI Polifenóis é amplamente divulgado na internet
Uma ação de fiscalização da Agência Nacional de Vigilância Sanitária (Anvisa) determinou a apreensão do chá misto Protocolo RMGI Polifenóis, da empresa Equilibrium Marketing Ltda. A medida, publicada nesta quinta-feira (2/2), proíbe qualquer tipo de comércio, distribuição, fabricação, divulgação e consumo.
O produto, vendido e divulgado na internet, é fabricado por empresa irregular. Após inspeção feita pela Anvisa e pela Vigilância Sanitária de Minas Gerais, foi constatado que o produto era fabricado em um galpão clandestino, sem alvará sanitário, na cidade de Arcos (MG). Na rotulagem, consta que a produção está a cargo da Wevj Industria de Suplementos Ltda
Confira a Resolução (RE) 1.271/2026, no Diário Oficial da União.
Serviços de internet da Anvisa passarão por manutenção programada no sábado (4/4)
A ação tem como objetivo melhorar a qualidade, a estabilidade e o desempenho da rede da Agência
Informamos que será realizada manutenção programada nos serviços de internet da Agência Nacional de Vigilância Sanitária (Anvisa) no próximo sábado (4/4), a partir das 8h, com duração estimada de até três horas.
Durante esse período, alguns serviços e sistemas poderão ficar temporariamente indisponíveis. A ação tem como objetivo melhorar a qualidade, a estabilidade e o desempenho da rede da Agência.
Recomendamos que as atividades que dependam desses serviços sejam realizadas com antecedência.
Destacamos que serviços que operam em nuvem, tais como: correio eletrônico, Sharepoint, OneDrive permanecerão operacionais durante toda a manutenção.
Agradecemos a compreensão de todos.
Declaração do Rio de Janeiro: compromisso inédito pela convergência de processos regulatórios na América Latina
Documento foi assinado por representantes do Chile, da Colômbia, de Cuba, do México, do Paraguai, do Panamá e do Brasil

A assinatura da Declaração do Rio ocorreu durante o "Diálogo Internacional em Saúde", no Rio de Janeiro
O diretor-presidente da Agência Nacional de Vigilância Sanitária (Anvisa), Leandro Safatle, abriu a 5ª Reunião Pública da Diretoria Colegiada de 2026 da última quarta-feira (1º/4) destacando a participação da Agência no evento "Diálogo Internacional em Saúde", realizado no Rio de Janeiro, na última semana.
Safatle falou sobre a assinatura da Declaração do Rio de Janeiro, referendada pelas autoridades reguladoras do Chile, da Colômbia, de Cuba, do México, do Paraguai, do Panamá e do Brasil. Segundo ele, o documento é uma aliança estratégica entre as principais autoridades sanitárias da América Latina, foi firmada com objetivo de fortalecer a vigilância e a proteção da saúde pública na região.
A Declaração do Rio de Janeiro estabelece um compromisso inédito de cooperação técnica e confiança mútua, fundamentado em evidências científicas e na transparência institucional. O documento busca convergência dos países signatários em uma base sólida para processos regulatórios.
Leia a íntegra da Declaração do Rio de Janeiro
“A Declaração do Rio de Janeiro é clara ao reconhecer que a região é diversa em contextos institucionais, marcos legais e níveis de maturidade regulatória, mas também é enfática ao afirmar que a cooperação e o fortalecimento de capacidades regionais são o caminho para superar essas simetrias”, enfatizou Safatle.
Com esse compromisso, os gestores reafirmam que a união de esforços é o caminho mais seguro para proteger a população e construir um futuro resiliente, onde a colaboração técnica sobrepõe-se às barreiras geográficas em prol da vida.
Resiliência dos sistemas de saúde
O objetivo central da declaração é a ampliação da resiliência dos sistemas de saúde, por meio da promoção da confiança regulatória, ampliação da cooperação e fortalecimento da região. Por meio de princípios de boa-fé e responsabilidade, as autoridades buscam otimizar as capacidades regionais, permitindo o aproveitamento compartilhado de inspeções e conhecimentos técnicos. Essa integração estratégica visa não apenas a eficiência na gestão de recursos, mas também o fortalecimento das instituições locais frente aos desafios globais de saúde.
A operacionalização desta rede baseia-se na adoção de boas práticas regulatórias internacionais, com foco em análise de riscos, rastreabilidade e gestão da qualidade. O intercâmbio ágil de informações técnicas é um pilar essencial do acordo, operando sob rigorosos protocolos de confidencialidade e segurança jurídica. As autoridades compreendem que a confiança institucional é um ativo construído por meio de decisões tecnicamente robustas, sendo o alicerce necessário para uma infraestrutura regional de alta performance.
No plano internacional, a declaração projeta a América Latina como um bloco mais coeso e influente em fóruns multilaterais. Ao atuar de forma solidária, os países signatários asseguram uma participação mais equilibrada nos mecanismos globais de saúde, promovendo medidas que mitigam riscos sanitários em larga escala. A cooperação é apresentada como a ferramenta indispensável para elevar os padrões de segurança e eficácia de produtos e serviços em todo o continente.
Anvisa determina apreensão de lotes falsificados de Mounjaro
Outros produtos sem registro sanitário também estão proibidos
A Agência Nacional de Vigilância Sanitária (Anvisa) determinou, nesta quinta-feira (2/4), a apreensão do lote D856831 do medicamento Mounajro e os lotes D880730, D840678 do Mounajro Kwikpen, fabricados por empresa não identificada. A medida proíbe também a comercialização, distribuição e o uso dos produtos falsos.
A empresa detentora do registro do medicamento, Eli Lilly Brasil, informou que foram encontrados, no mercado, unidades desses lotes com características diferentes do produto original, o que indica falsificação.
Entre os problemas identificados estão número de série não identificados nos sistemas da empresa, uso de material diferente do original na embalagem e falha na leitura do código 2D.
Empresa não identificada
Outro item que sofreu ação fiscal foi o medicamento Tirzec, produzido por empresa não identificada. O produto irregular deve ser apreendido e estão proibidas sua comercialização, distribuição, fabricação, importação, divulgação e utilização. Foi constatado que o produto anunciado não tem registro, cadastro ou notificação na Anvisa.
Também foi determinada a apreensão do produto Skin body Organic, da linha Eros. Fabricado pela empresa Skin & Body Nutracêuticos e Cosméticos Organic Ltda., os itens não podem ser comercializados, distribuídos, fabricados, importados e utilizados. A medida foi tomada após comprovação da comercialização e divulgação de produtos sem registro, notificação ou cadastro na Anvisa.
Confira a Resolução (RE) 1.279/2026 no Diário Oficial da União.
Diretoria da Anvisa amplia lista de medicamentos radiofármacos
O assunto foi um dos destaques da 5ª Reunião Pública da Diretoria Colegiada de 2026, realizada na quarta-feira (1º/4)

5ª Reunião Ordinária Pública da Diretoria Colegiada da Agência Nacional de Vigilância Sanitária (Anvisa) de 2026,
realizada no edifício-sede da organização, em Brasília (DF) – Foto: Jacqueline Spotto/Anvisa
Nesta quarta-feira (1º/4), os diretores da Agência Nacional de Vigilância Sanitária (Anvisa) realizaram a 5ª Reunião Pública da Diretoria Colegiada (ROP5) de 2026, sob a presidência do diretor-presidente, Leandro Safatle.
Onze itens integravam a relação de assuntos deliberativos de regulação previstos na ROP5. Entre eles estava a proposta de prorrogação do prazo para envio de contribuições às Consultas Públicas nos 1.362 a 1.368/2025, que tratam de revisão dos requisitos higiênicosanitários e de boas práticas de fabricação para estabelecimentos produtores ou fabricantes de alimentos.
Em 20 de março, por meio de decisão monocrática, o relator do caso, diretor-presidente, Leandro Safatle, havia proferido inicialmente, em caráter de urgência, a extensão do prazo. O período, a princípio, se encerraria no fim de março. Nesta quarta-feira (1°/4), ele apresentou a proposta para que o colegiado a referendasse.
As propostas normativas em discussão buscam atualizar as regras de Boas Práticas de Fabricação (BPF) e os procedimentos operacionais padronizados para diversos segmentos, incluindo suplementos alimentares, fórmulas nutricionais, águas envasadas, amendoins processados, gelados comestíveis e conservas de frutas e hortaliças.
Segundo Safatle, a complexidade técnica dos textos exige mais tempo para análise por parte das vigilâncias sanitárias locais e de grupos sociais potencialmente impactados, com destaque para a agricultura familiar e povos e comunidades tradicionais. "A participação qualificada tende a produzir contribuições mais consistentes, lastreadas na realidade concreta dos estabelecimentos produtores e nas capacidades institucionais dos órgãos de vigilância", frisou.
De forma unânime, os diretores referendaram a decisão e as consultas públicas seguem abertas até o final de maio.
Ampliação da lista de radiofármacos
Outro item aprovado pela diretoria foi a atualização da instrução normativa (IN) com as listas de radiofármacos que podem ter a sua comprovação de eficácia e segurança comprovados por meio de dados externos. Isso significa que o registro de medicamentos radiofármacos da lista podem ser feitos com base em estudos clínicos publicados em revistas indexadas, em casos que foram estudadas as mesmas atividades e mesmas indicações terapêuticas ou diagnósticas que a empresa pede no registro. Esta forma de comprovação está prevista na Resolução da Diretoria Colegiada (RDC) 738/2022.
A medida garante a ampliação dos medicamentos que são fundamentais para diagnóstico e tratamento.
Atualmente, a regulamentação aplicada a medicamentos radiofármacos é composta por três atos normativos principais: a RDC 738/2022, que apresenta os requisitos para notificação, registro e importação desses produtos; a IN 319/2024, que detalha a documentação necessária para o protocolo de registro desses produtos; e a IN 81/2020, que regulamenta a lista de medicamentos passíveis de apresentarem dados de literatura para comprovação da segurança eficácia.
Relatora da matéria, a diretora Daniela Marreco destacou que nos últimos quatro anos, o setor de radiofármacos passou a apresentar expansão gradual, com a entrada de novas empresas e produtos. Segundo ela, a atualização dessa lista é estratégica, não apenas para refletir a realidade atual do mercado, mas também para fomentar o registro de novos medicamentos, o que ampliará o acesso a produtos devidamente regularizados e incentivará a inovação no setor.
Aprovada por unanimidade, a nova norma ampliará a lista de 33 para um total de 57 radiofármacos.
Silicone
Também por decisão unânime, a diretoria referendou uma RDC e uma IN para a regulação dos requisitos sanitários aplicáveis aos silicones utilizados em materiais, embalagens, revestimentos e equipamentos destinados a entrar em contato com alimentos. A preocupação principal é a possibilidade de as substâncias contidas nesses materiais migrarem para o alimento e serem ingeridas pelos consumidores.
“Os materiais de silicone vêm ganhando espaço no mercado, em especial, no mercado de materiais que entram em contato com alimentos para diversas finalidades. Incluem-se aí bicos de mamadeiras, assadeiras, utensílios para congelar alimentos e espátulas”, enumerou o diretor relator Marcelo Moreira.
Como o interesse comercial pelo material está em crescimento, a Agência estabeleceu regras específicas para o uso. O relator destacou que a definição das substâncias que podem ser empregadas nos produtos garante a segurança dos consumidores e traz clareza e segurança jurídica para as empresas.
Enquanto a RDC aprovada dispõe sobre os requisitos sanitários aplicáveis aos silicones utilizados, a IN estabelece as definições, as listas de substâncias autorizadas e os métodos analíticos aplicáveis à elaboração do material.
»Veja mais fotos da 5ª Reunião Pública da Diretoria Colegiada de 2026 no Flickr da Anvisa
Reveja a reunião no canal da Anvisa no YouTube
Anvisa integra operação Bula Fria contra rede criminosa de medicamentos oncológicos
Além da Agência, ação conjunta nesta quinta-feira (2/4) envolve Polícia Federal, Receita Federal e Ministério Público Federal

Foto: PF
Nesta quinta-feira (2/4), Agência Nacional de Vigilância Sanitária (Anvisa), Polícia Federal (PF), Ministério Público Federal (MPF) e Receita Federal do Brasil (RFB) deflagraram a Operação Bula Fria, direcionada à desarticulação de organização criminosa dedicada à comercialização ilícita de medicamentos oncológicos de alto custo no território nacional, que envolve sérios riscos sanitários.
As investigações revelaram um esquema altamente estruturado de introdução clandestina de medicamentos sem registro sanitário no Brasil, inclusive produtos para tratamento de câncer.
Os crimes sob investigação incluem contrabando, falsificação, corrupção, adulteração ou alteração de produto destinado a fins terapêuticos ou medicinais, crimes contra a ordem tributária e lavagem de capitais.
Fonte: Anvisa, em 02.04.2026.
